Anvisa autoriza estudo clínico de vacina contra covid da Inovio Pharmaceuticals
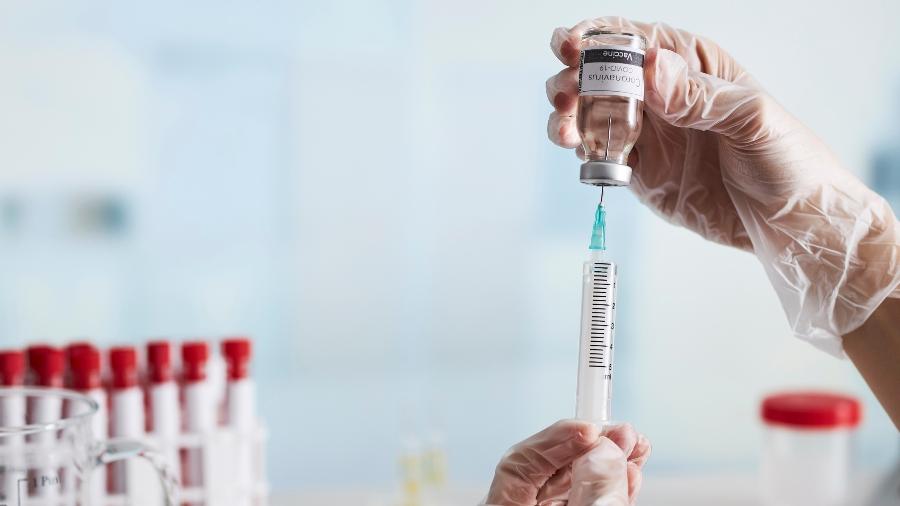
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou hoje a realização de ensaio clínico no Brasil da vacina INO-4800 contra a covid-19. O ensaio clínico é patrocinado pela empresa americana de Biotecnologia Inovio Pharmaceuticals e o imunizante será administrado por via intradérmica (ID).
De acordo com a agência reguladora, o ensaio é de Fase 3, controlado por placebo. Um a cada três voluntários receberá o placebo para avaliar segurança, imunogenicidade e eficácia da candidata à vacina. No local de aplicação da vacina será utilizada uma técnica de facilitação para entrada do DNA no tecido celular (eletroporação) com um dispositivo próprio.
O estudo prevê aplicação de duas doses com intervalo de 28 dias em voluntários maiores de 18 anos. O protocolo estima a participação de 350 voluntários no Brasil distribuídos entre os Estados do Rio de Janeiro, São Paulo, Santa Catarina e Rio Grande do Sul.
Além do Brasil, o ensaio conta com 7.116 participantes também distribuídos na Argentina, Colômbia, Estados Unidos, Filipinas, México, Peru, Polônia, República Checa e Tailândia. Os estudos iniciais de Fase 1 e 2 foram realizados nos Estados Unidos, Coreia do Sul e China.















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.