Laboratório agenda reunião com governo para fornecimento do rendesivir
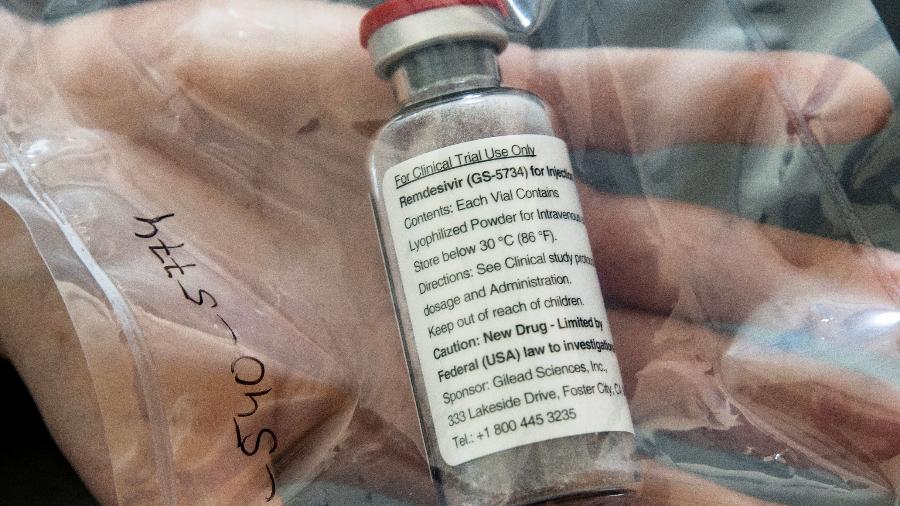
O laboratório Gilead, fabricante do rendesvir, marcou uma reunião com o Ministério da Saúde para acertar o fornecimento do medicamento, aprovado na última sexta-feira pela Anvisa (Agência Nacional de Vigilância Sanitária) para tratamento da covid-19. De acordo com o jornal Valor Econômico, o laboratório vai negociar diretamente com a pasta preço, quantidade e cronograma de entrega.
Este é o primeiro remédio aprovado para uso contra o novo coronavírus. A autorização foi dada apenas para uso hospitalar e para pacientes com mais de 12 anos, com quadro de pneumonia e que precisam de oxigênio. Estudos com o fármaco mostraram recuperação mais rápida dos pacientes internados.
Com nome registrado de Veklury, o remédio é um antiviral desenvolvido para vírus como Ebola, mas que passou a ser considerado para o tratamento da covid-19.
Segundo a Anvisa, o remédio já foi autorizado por autoridades sanitárias em mais de 20 países, entre eles, Argentina, Estados Unidos, Índia, Israel, Japão, Rússia, Coreia do Sul e Canadá, além de ter recebido a permissão da agência europeia.
Entre fevereiro e maio de 2020, foram realizados estudos clínicos (nas fases 1, 2 e 3) com 6.283 pacientes, entre homens e mulheres com infecção pelo novo coronavírus comprovada por exames laboratoriais. Os testes clínicos foram realizados em 10 países, não no Brasil.
No estudo, os participantes que receberam o remédio tiveram um tempo de recuperação menor, de dez dias, contra 15 dias daqueles que não receberam a substância. Os eventos adversos não foram maiores no grupo que recebeu o rendesivir do que entre os que não tiveram o remédio aplicado.
Segundo a Anvisa, os estudos demonstram que "o tratamento com rendesivir pode prevenir uma progressão da doença causada pelo coronavírus de 2019 (COVID-19) em adultos e adolescentes (com idade igual ou superior a 12 anos e com peso corporal de, pelo menos, 40 kg) com pneumonia que requerem administração suplementar de oxigênio (oxigênio de baixo ou alto fluxo, ou outra ventilação não invasiva no início do tratamento), como demonstrado nos estudos, através do menor tempo de recuperação no grupo rendesivir".
O tratamento deve ser realizado por, pelo menos, cinco dias e não mais do que dez. Para obter êxito, o remédio deve ter aplicação inicial de 200g no primeiro dia e outras doses de 100 mg nos dias seguintes. A forma de aplicação é intravenosa.
Polêmica e OMS
Em novembro de 2020, a Organização Mundial da Saúde (OMS) publicou uma recomendação contra o uso do rendesivir para o tratamento da covid-19. O comunicado foi emitido a partir da avaliação de que não havia evidências da eficácia do remédio no tratamento da doença.
A posição foi feita por um grupo internacional de desenvolvimento de diretrizes, com médicos e outros profissionais da saúde. O grupo analisou quatro estudos que envolveram o impacto do rendesivir em 7 mil pacientes.
Apesar da recomendação contrária da OMS, a Anvisa esclareceu que avaliou aspectos diferentes ao liberar o medicamento no Brasil. Além disso, a situação crítica da pandemia no país e o colapso do sistema de saúde em vários lugares contaram para a avaliação.
"O estudo da OMS avaliou mais a ocorrência de mortalidade e pacientes com perfil um pouco diferente dos avaliados nos outros estudos que consideramos para liberar o remédio. O estudo que consideramos válido focou na redução do tempo de hospitalização dos pacientes e vimos que houve uma redução na hospitalização", disse a gerente de avaliação de segurança e eficácia da Anvisa, Renata Soares.
*Com informações da Agência Brasil















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.