Saúde tentou importar vacina indiana prestes a vencer, diz jornal
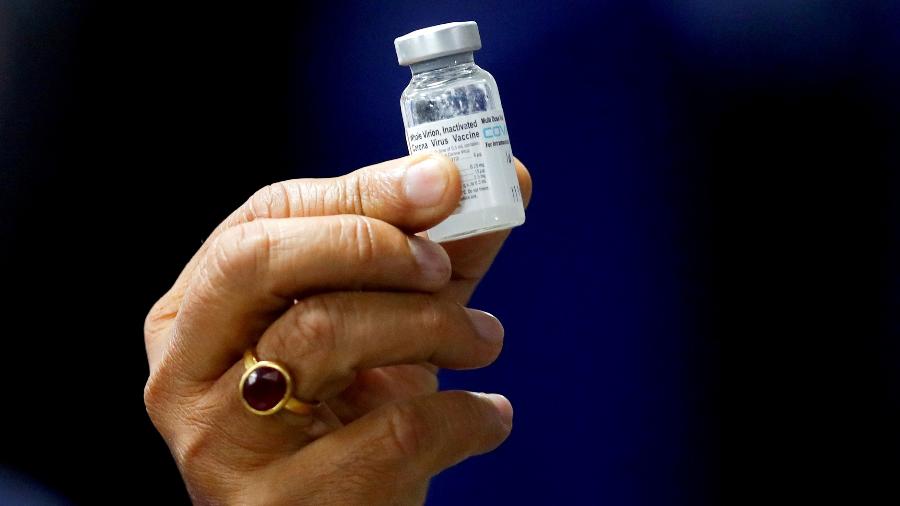
O Ministério da Saúde tentou comprar três lotes da vacina indiana Covaxin com prazo de validade perto do fim. Os imunizantes seriam utilizados na campanha nacional de vacinação contra a covid-19. A informação foi divulgada pelo jornal O Globo.
O contrato, orçado em R$ 1,6 bilhão, para aquisição de 20 milhões de doses foi firmado pela pasta em fevereiro, sob a gestão do general Eduardo Pazuello. A transação com a Precisa Medicamentos (representante no país do laboratório indiano Bharat Biotech) é investigada pelo MPF (Ministério Público Federal). Os promotores apuram detalhes do contrato e se a empresa terá condições de fornecer os produtos conforme o prometido.
O acordo prevê o envio de cinco remessas de quatro milhões de vacinas de forma escalonada. As entregas começariam em março e terminariam em meados de junho. No entanto, a importação do produto está paralisada desde 31 de março, após negativa da Anvisa (Agência Nacional de Vigilância Sanitária).
Antes do veto, no dia 23 de março, o governo federal deu início ao processo de importação. O Ministério da Saúde remeteu à Anvisa informações detalhadas sobre os lotes que seriam importados. Durante a verificação da documentação, técnicos da agência constataram que, considerando a data de fabricação dos lotes, os imunizantes venceriam entre abril e maio.
No mesmo dia, a Anvisa pediu esclarecimentos à pasta.
"O prazo de validade aprovado pela autoridade indiana para a vacina Covaxin é de 6 meses, se conservada em 2-8 °C. De acordo com as datas de fabricação dos lotes a serem importados, observa-se que o prazo de validade irá expirar nos meses de abril e maio/2021. Solicita-se esclarecer se é possível a utilização de todo o quantitativo previamente à data de expiração dos lotes", diz o ofício.
Em resposta a solicitação, a Precisa Medicamentos confirmou que a validade da vacina era de seis meses, conforme preconizado pelas autoridades indianas. Entretanto, a farmacêutica afirmou haver novos estudos que indicariam a possibilidade de armazenamento por um tempo maior, sem especificar que pesquisas seriam essas.
A diretora técnica da empresa, Emanuela Medrades, argumenta que a Precisa se comprometia a assinar um termo de compromisso para que nenhuma vacina chegasse ao Brasil com mais de 30% do seu prazo de validade transcorrido.
"Sobre o parágrafo 3, item IV, o prazo de validade aprovado pela autoridade indiana para a vacina Covaxin é de 6 meses, se conservada de 2 a 8ºC, porém, os estudos de estabilidade acelerada já avançaram tal período. Dessa forma, a Precisa Medicamentos apresenta a possibilidade de assinatura de um termo de compromisso assegurando que nenhum produto importado terá percorrido mais que 30% de sua validade", traz o documento.
Informações divergentes para conseguir importar
Para que a vacina pudesse ser importada, o Ministério da Saúde teria de cpnseguir uma licença junto ao Siscomex (Sistema de Comércio Exterior), vinculado à Receita Federal, e uma autorização da Anvisa.
Porém, técnicos da Anvisa encontraram informações distintas aos dois órgãos.
A pasta informou ao Siscomex que o número do lote a ser trazido ao país era o nº 37F21004A, correspondente a três milhões de doses avaliadas em R$ 243 milhões. Já para a Anvisa, o ministério informou que iria importar três lotes diferentes do que foi informado ao Siscomex: 37620001A, 37620002A e 37620003A.
A anuência de importação é chancelada de forma específica para os lotes informados, depois de vistoria feitra pela Anvisa afim de averiguar as condições de fabricação de cada um deles.
Os documentos também mostram que o Ministério da Saúde teria transmitido informações equivocadas sobre o prazo de validade do lote nº 37F21004A ao solicitar a licença de importação junto ao Siscomex. A pasta informou que o prazo de validez da remessa seria até janeiro de 2023. Os técnicos alertaram a pasta sobre a irregularidade.
"Ademais, no LI (licenciamento de importação) consta a data de validade do lote 37F21004A como sendo 01/2023. No entanto, o prazo de validade aprovado pela Autoridade Indiana para a vacina Covaxin é de 6 meses, se conservada de 2-8 °C. Portanto, a data de validade do referido lote não corresponde ao prazo de validade aprovado pela autoridade da Índia", diz o ofício.
O que dizem os envolvidos?
Questionada, a Precisa Medicamentos disse que que os lotes informados durante a licença de importação se referiam aos produtos que estavam disponíveis para envio ao Brasil em março. Segundo a empresa, esses lotes já teriam sido utilizados e não virão ao Brasil.
A empresa também afirma que não há risco de enviar vacinas perto do prazo de validade para o país, por conta de previsões contratuais.
"Não há nenhum risco de se importar lotes com vacinas próximo à validade porque está estabelecido em contrato que nenhum lote será enviado ao Brasil com validade inferior a 70% do prazo final, o que garante tempo suficiente para a distribuição e aplicação", destacou.
Já o Ministério da Saúde garantiu nunca ter adotado a "estratégia" de importar produtos "com prazo exíguo".
"Nunca foi estratégia a importação de produtos com prazo exíguo, inclusive o que seria vedado em virtude do próprio contrato", afirma a pasta.
Quanto a validade dos lotes, a pasta afirma que o assunto já foi tratado junto à Anvisa.
"Acerca da validade dos frascos e da discrepância das informações entre Siscomex e Anvisa todas já foram esclarecidas em reuniões posteriores entre Ministério, Anvisa e equipe técnica da empresa, e tiveram sua origem em virtude do envio parcial de documentos", traz a nota.
Ainda segundo o ministério, um novo pedido de importação da Covaxin deve acontecer nos próximos dias.
A Anvisa disse que já deliberou esse primeiro pedido de importação da Covaxin e que sua diretoria decidiu por não autorizar o pedido. E também que novos pedidos podem sim ser apresentados a qualquer momento.
"As vacinas devem ser importadas e utilizadas dentro de seu prazo de validade. Cabe ao importador verificar se os lotes a serem importados possuem um prazo de validade adequado considerando a expectativa com relação ao prazo para sua utilização após chegada ao Brasil", informou a agência.














ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.