Plano de imunização só ficará pronto com vacina aprovada, diz secretário

Arnaldo Medeiros, Secretário de Vigilância em Saúde do Ministério da Saúde, disse hoje que o plano de vacinação contra a covid-19 só ficará pronto e fechado quando a vacina estiver registrada na Anvisa. O governo tem adiado com frequência a divulgação desse planejamento. Existe a expectativa de que saia uma versão prévia ainda nesta semana.
"É fundamental pensarmos que esse plano operacional para a vacinação da covid-19 só ficará definitivamente pronto, fechado, quando tivermos uma vacina ou mais de uma, que esteja registrada na Anvisa", disse Medeiros, em entrevista coletiva que tratava sobre outro tema, o combate à Aids.
Ele confirmou que o Ministério da Saúde terá uma reunião sobre vacinação ainda hoje para definir alguns itens do plano de vacinação.
"Nós estamos avançando com o plano de imunização para covid-19 e devemos ter os resultados ainda esta semana sobre os 10 eixos", prometeu o secretário.
Esses 10 eixos devem definir, por exemplo, o público-alvo prioritário e também decidir como será a distribuição das doses. O Ministério da Saúde precisa resolver se vai entregar as vacinas de acordo com a gravidade da pandemia em cada local.
Perfil da vacina
Por enquanto, o governo federal não comprou nenhuma vacina, apesar de o presidente Jair Bolsonaro (sem partido) já ter assinado uma Medida Provisória com intenção de compra da vacina de Oxford/Astrazeneca no valor de R$ 1,9 bilhão. Na entrevista de hoje, Medeiros falou qual é o tipo de imunizante desejado, reduzindo as possibilidades diante dos imunizantes apresentados até agora.
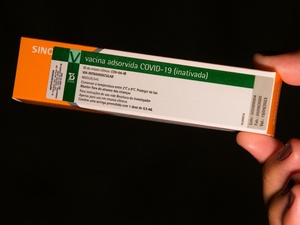
"Desejamos que a vacina seja fundamentalmente termoestável por longos períodos, em temperaturas de 2 a 8 graus, porque a nossa rede de frios é montada e estabelecida com essa temperatura", disse o Secretário.
Ao priorizar uma vacina termoestável, o Brasil deve deixar de lado as primeiras vacinas que devem ser liberadas nos Estados Unidos e na Europa. São as vacinas da Pfizer (que exige armazenamento a -70º) e da Moderna (-20º), que não são termoestáveis, ou seja, não conseguem ficar estáveis sob temperatura de 2°C a 8°.
A vacina da Pfizer pode ser aprovada nos Estados Unidos em 10 de dezembro. Na Europa ela pode ser liberada em 29 de dezembro. Já a vacina da Moderna pode ser liberada em 17 de dezembro nos EUA e em 12 de janeiro na Europa.
O secretário ainda afirmou que a prioridade do governo seria comprar vacinas aplicadas em doses únicas. No entanto, os principais imunizantes que apresentaram até agora relatórios finais ou parciais de eficácia, são aplicados em duas doses: Oxford/Astrazeneca, Coronavac (Sinovac/Instituto Butantan), Pfizer/Biontech, Moderna e Sputnik V.















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.