Fiocruz zera pendência na Anvisa, e Butantan deve 3 dados; veja o que falta
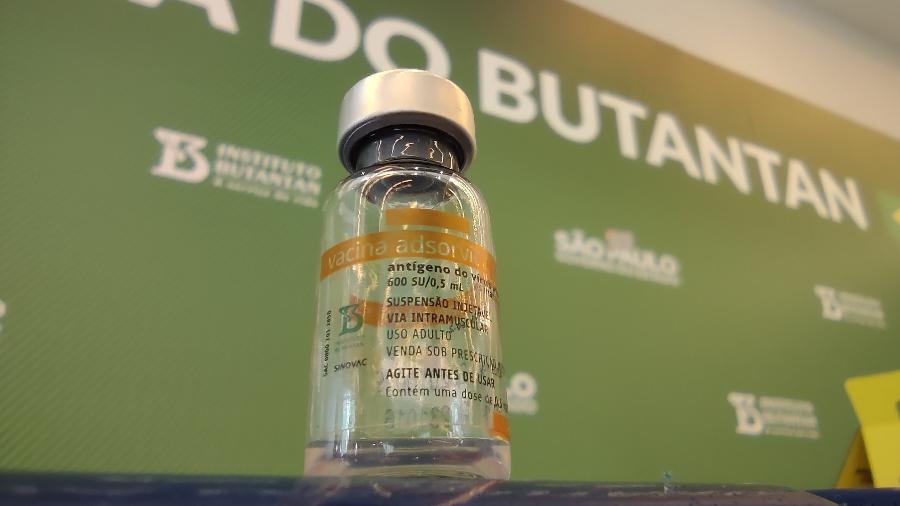
A Fiocruz zerou suas pendências com a Anvisa para o uso emergencial da vacina desenvolvida pelo laboratório AstraZeneca em parceria com a Universidade de Oxford. Já o Instituto Butantan, parceiro da chinesa Sinovac na produção da CoronaVac, deve três documentos —a data limite de entrega é o dia 28 de janeiro.
A falta desses dados, porém, não deve alterar a autorização já obtida pelo Butantan de vacinar grupos de risco — profissionais de saúde, idosos e indígenas. No domingo (17), a Anvisa autorizou o uso emergencial dos dois imunizantes, mas fez ressalvas a três documentos da Fiocruz e a quatro do Butantan.
Na manhã desta quarta, restava dessas demandas a entrega dados complementares de três documentos sobre Coronavac:
- Imunogenicidade - Falta enviar dados sobre a quantidade de anticorpos que cada quantidade de vacina produz no corpo humano. Saber isso permitirá que se use a menor quantidade possível de imunizante para gerar a mais quantidade possível de proteção
- Eficácia em diferentes grupos - É a eficiência da vacina em grupos específicos de voluntários, como idosos jovens, pessoas que já tiveram a doença ou que possuem comorbidades. "É um dado necessário para entender melhor de que forma cada perfil da população se beneficia da vacina e se a vacina teria eficácia aceitável em quem nunca teve a doença", afirmou a Anvisa.
- Validação dos testes - "São as informações sobre como são feitas as análises de imunogenicidade, ou seja, se o teste utilizado para medir a presença e a quantidade de anticorpos nos voluntários da pesquisa garante resultados confiáveis", disse a agências. "É importante porque a metodologia do teste e a sua confiabilidade têm impacto na interpretação dos resultados."
Até o momento, nenhum laboratório fez o pedido de registro de vacina na Anvisa, o que permitirá que os imunizantes possam ser aplicados em qualquer pessoa.
Há uma expectativa de que a Fiocruz faça a requisição nesta semana. O laboratório, porém, ainda não recebeu os primeiros 2 milhões de doses da vacina da AstraZeneca/Oxford, que seriam importadas da Índia na semana passada.
Já o Butantan, que entregou às autoridades brasileiras 6 milhões de doses da Coronavac, aguarda a liberação de outros 4,8 milhões, informou que entregará os documentos pendentes dentro prazo.
Informações melhorariam aplicação de vacinas
A assessoria da Anvisa informou que as informações pendentes não se prestam a confirmar a segurança das vacinas. "Nenhuma das ressalvas trata de questionamentos sobre a segurança das vacinas", disse a agência ao UOL. "[A segurança] está bem demonstrada nos estudos. As ressalvas tratam basicamente de entender melhor a eficácia e se as vacinas [de Oxford fabricadas na Índia e no Reino Unido] são comparáveis."
Um servidor da agência que já trabalhou com liberação de vacinas acrescentou, reservadamente, que esse é um procedimento normal devido à complexidade do tema e à pandemia de coronavírus. Segundo ele, a busca de novos documentos serve de subsídio para identificar se algo precisa ser ajustado ou melhorado.
No caso do chamado "relatório de imunogenicidade", a Anvisa informou, no domingo passado, que o "dado é imprescindível para que se possa concluir a duração da resposta imunológica nos indivíduos vacinados".
O epidemiologista e ex-secretário de Vigilância em Saúde do Ministério da Saúde Wanderson Oliveira disse ao UOL que os documentos pendente pedidos pela Anvisa são importantes, mas não críticos. "Não são informações que vão causar nenhum prejuízo, como: 'Ah, eu não devia ter liberado' e fazer recuar", disse.
Segundo Oliveira, essas novas informações do uso emergencial das vacinas vão ser úteis para facilitar e acelerar o registro dos imunizantes.
Há outras vacinas em análise no Brasil, e ontem a Anvisa anunciou que concedeu certificado de boas práticas aos laboratórios Pfizer e Janssen.
Veja os outros documentos entregues hoje pelo Butanan e pela Fiocruz:
Butantan
- Intervalo de doses. A agência pediu, e recebeu, quais os intervalo entre as duas doses que produzem mais ou menos eficácia na vacinação. Isso permitirá informar na bula a melhor data para aplicar a segunda injeção no paciente e deixá-lo mais protegido.
Fiocruz
- Testes de pureza. Era preciso validar o método de análise dos testes de pureza nas vacinas porque é normal serem usadas substâncias para dar estabilidade ao produto, mas isso não pode passar de certos limites para, por exemplo, não atrapalhar a aplicação da vacina ou causar dor no paciente.
- Testes de estabilidade. Faltava saber se os lotes de uso emergencial são os mesmos em que foram feitos sobre os chamados testes de "estabilidade". Esses exames, entre outras coisas, determinam se "pozinhos" formados no fundo dos fracos desaparecem depois de uma sacudida pelos técnicos pouco antes da aplicação.
- Desenvolvimento de lotes e comparações. "A comparabilidade busca saber basicamente se a vacina do Serum é semelhante à vacina da Astra Zeneca", disse a Anvisa. "Isso é importante porque qualquer mudança de método, equipamento, local de fabricação e até mesmo de equipe, pode impactar a qualidade do produto".
Fontes: Anvisa e epidemiologista Wanderson Oliveira















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.