Moderna vai pedir à Anvisa para usar vacina de covid em bebês de 6 meses
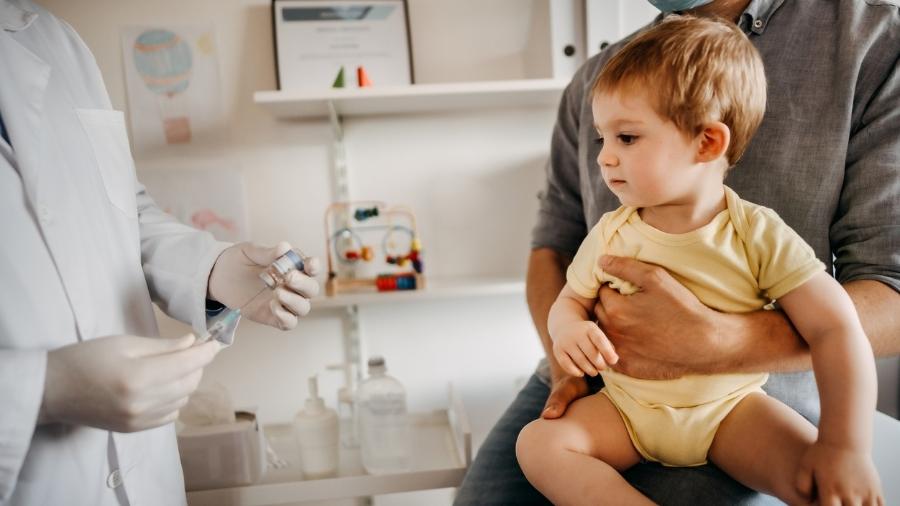
A Zodiac, representante da farmacêutica Moderna no Brasil, vai pedir o registro definitivo na Anvisa (Agência Nacional de Vigilância Sanitária) da vacina contra a covid-19. A intenção é conseguir autorização para aplicar o imunizante em pessoas a partir dos 6 meses de idade.
A representante informou ao UOL que ainda não há uma data definida para o pedido e que por enquanto o processo está na fase de montagem do dossiê exigido pela Anvisa. No entanto, a Zodiac diz que o pedido deve ser entregue ainda este semestre e afirma esperar que a vacina esteja disponível no Brasil até o final deste ano.
No início de abril, a Anvisa realizou uma reunião técnica com a Zodiac e a Moderna para tratar da regularização da vacina. Hoje em dia, a vacina da Moderna não tem nenhum tipo de autorização para uso no Brasil, mas é usada em adultos em 85 países e também tem autorização emergencial da OMS (Organização Mundial de Saúde).
Entre os imunizantes contra covid-19 aprovados no Brasil, apenas dois são utilizados em crianças. O da Pfizer a partir de 5 anos de idade e a CoronaVac a partir de 6 anos. O Instituto Butantan, responsável pelo desenvolvimento da CoronaVac no Brasil, tenta conseguir a aprovação para uso da vacina em crianças a partir de 3 anos.
A Moderna está testando o uso no população infantil. Segundo a empresa, os resultados da segunda fase do estudo, anunciados em 23 de março, "mostraram uma resposta robusta de anticorpos neutralizantes na faixa etária de 6 meses a menos de 6 anos, juntamente com um perfil de segurança favorável".
"Acreditamos que a mRNA-1273 será capaz de proteger com segurança essas crianças contra o SARS-CoV-2, e isso é muito importante em nossa luta contínua contra a covid-19, e será especialmente bem aceita pelos pais e cuidadores", disse Stéphane Bancel, presidente corporativo da Moderna.
Uma solicitação similar com a que está sendo preparada para o envio à Anvisa já foi feita junto ao FDA (Food and Drug Administration), a agência reguladora dos Estados Unidos. Lá, porém, o pedido é para uso emergencial.















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.