Caso vacina seja eficaz, SP pedirá liberação emergencial à Anvisa em outubro
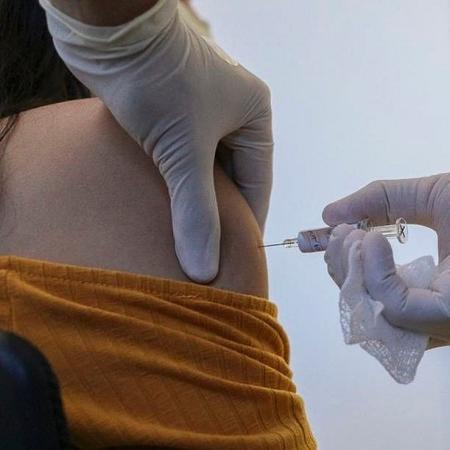
Diante de uma possível efetividade da vacina Coronavac, o governo de São Paulo pode pedir à Anvisa uma liberação emergencial do imunizante ainda em outubro. A vacina está em fase de testes em humanos no Brasil e é uma parceria do Instituto Butantã com a chinesa Sinovac.
"A informação foi divulgada em entrevista coletiva, hoje (12), pelo secretário estadual da Saúde de São Paulo, Jean Gorinchteyn. Segundo ele, esse pedido acontecerá se o resultado dos testes for positivo após três meses da aplicação, iniciada em julho."Agora, até outubro de 2020, se nós consagrarmos e confirmarmos que essa vacina é segura, ou seja, mantém a característica de não levar a efeitos colaterais e produzir anticorpos por um período prolongado, altos e mantidos nos próximos três meses, aí sim, nós teremos a possibilidade, de forma emergencial para a Anvisa que haja então a possibilidade de nós usarmos na população", disse durante coletiva de imprensa realizada no Palácio dos Bandeirantes. O governador João Doria (PSDB) cancelou participação no evento após ser diagnosticado com a covid-19.
"É importante nós lembrarmos que São Paulo precisa de uma vacina, seja ela da Sinovac, seja de Oxford. Nós queremos uma vacina porque é a única forma de poderemos voltar para aquela condição de normal. Por enquanto, estamos longe até desse 'novo normal', isso ainda está distante", reiterou.
Ontem (11), Doria comentou que não haveria motivo para o Instituto Butantã trabalhar também com a vacina russa, que foi regulamentada nesta semana pelo governo de Vladimir Putin. Segundo Gorinchteyn, é necessário respeitar todas as fases de testagem para atestar que o produto é eficaz e não impõe risco à população. "É importante nós sempre frisarmos que todas as vacinas devem e deverão seguir todos os preceitos éticos, de segurança e de eficácia, e isso é avaliado através de estudos científicos", apontou.
O secretário pontuou que, durante a fase anterior de testes, os voluntários chineses relataram apenas "pequenos" efeitos colaterais, como dor no local de aplicação e febre baixa. Os voluntários brasileiros serão acompanhados por um ano.
A vacina foi criada pelo laboratório chinês Sinovac Biotech. No Brasil, será testado em cerca de 9 mil voluntários em 12 centros de pesquisa dos Estados de São Paulo, Rio Grande do Sul, Minas Gerais, Rio de Janeiro e Paraná, além do Distrito Federal. O custo da testagem é estimado em R$ 85 milhões e prevê a transferência de tecnologia para que a vacina chinesa possa ser produzida em São Paulo, no Instituto Butantã. Os testes começaram em 21 de julho, no Hospital das Clínicas, e outros centros de pesquisa, como o Emílio Ribas, também já estão participando.

















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.