Butantan se reúne hoje às 16h com Anvisa para pedir registro de Coronavac
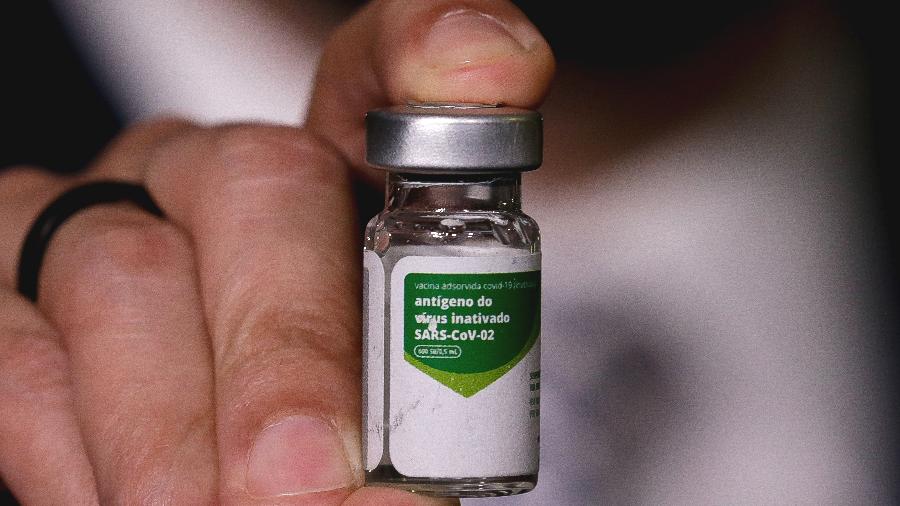
Os diretores do Instituto Butantan e da Secretaria de Saúde de São Paulo vão entregar hoje, às 16h, os estudos finais da vacina contra o novo coronavírus à Anvisa (Agência Nacional de Vigilância Sanitária) e pedir o registro da CoronaVac. O encontro virtual será com técnicos da agência e com o diretor da Gerência de Medicamentos e Produtos Biológicos, Gustavo Mendes.
A reunião para apresentar os estudos e pedir o registro de vacinação está marcada para o mesmo horário em que o governo de São Paulo anunciou uma entrevista a jornalistas para falar sobre o estudo.
O governador João Doria (PSDB) não estará presente na reunião nem na coletiva, ele viajou ontem à noite para Miami, mas decidiu hoje voltar a São Paulo após saber que o vice-governador Rodrigo Garcia (DEM) está com covid. O presidente da Anvisa, Barra Torres, não participará da reunião.
"Vamos nos reunir com a Anvisa para entregar os resultados dos estudos e depois apresentar os dados em coletiva para imprensa e para todo mundo", disse ao UOL o secretário de Saúde de São Paulo, Jean Gorinchteyn, que participará da reunião.
O governador João Doria prometeu o início da vacinação em 25 de janeiro. Mas depende de aval da Anvisa para aplicar doses.
Além da Anvisa, o governo paulista enviará os estudos à agência sanitária chinesa - National Medical Products Administration. A expectativa do governo João Doria (PSDB) é conseguir o registro junto aos chineses em até três dias. Com isso, se basear em uma lei aprovada este ano que determina prazo de 72 horas para Anvisa aprovar o uso de fármacos, desde que registrado em agências sanitárias internacionais. Entre essas agências, está a chinesa.
A CoronaVac é desenvolvida em parceria com o laboratório chinês Sinovac
O país registra 188.285 mortes em decorrência do novo coronavírus. Os dados foram divulgados ontem (22) pelo consórcio de veículos de imprensa, do qual o UOL faz parte.
Até o início desta tarde, não havia nenhum pedido de vacinação emergencial (para grupos de risco) ou registro (que libera a aplicação de doses para toda população) na Anvisa.
Guerra da Vacina
Nos bastidores, integrantes da Anvisa afirmam que mesmo com uma estrutura de plantão preparada para analisar os documentos talvez não seja possível conceder a aprovação em 72 horas, como prevê a lei. Isso porque, argumentam, a qualidade das informações fornecidas é fundamental.
Há divergências ainda sobre a necessidade ou não de um aval da Anvisa para que o governo paulista consiga até mesmo o registro na China. A Anvisa entende que por regular a pesquisa no país em que há o estudo mais amplo sobre a CoronaVac, cabe a agência enviar informações para análise do pedido na China.
De acordo com integrantes da Anvisa ouvidos pela reportagem, houve falha na documentação entregue por São Paulo ao longo do estudo. Por isso há o receio na agência de que, em meio à politização, haja uma pressão do governo paulista e uma tentativa de culpar a Anvisa de lentidão.
Integrantes do governo de São Paulo negam que exista pendência de documentos das fases iniciais dos estudos.
















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.