Reunião que avaliará uso emergencial de vacinas deve durar 5h, diz Anvisa
A Anvisa (Agência Nacional de Vigilância Sanitária) informou hoje (16) que a reunião marcada para amanhã (17) com o intuito de avaliar os pedidos de uso emergencial das vacinas contra a covid-19 deve durar pelo menos cinco horas. O encontro vai começar às 10h e será transmitido ao vivo pelo UOL.
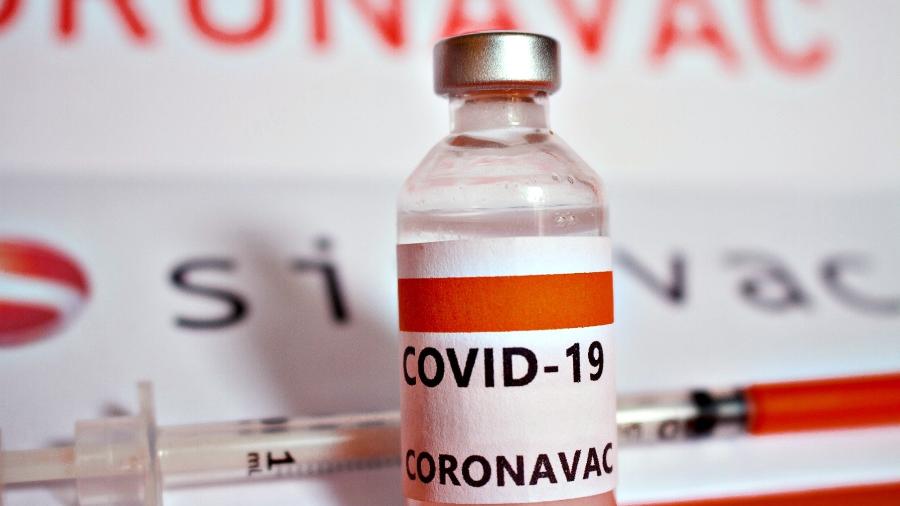
Dois imunizantes estão na pauta da Anvisa: a CoronaVac, fabricada e desenvolvida pelo Instituto Butantan em conjunto com a farmacêutica Sinovac; e a da Fiocruz, que é resultante de estudos da Universidade de Oxford, na Inglaterra, em parceria com o laboratório AstraZeneca.
Além da live disponibilizada pelos canais de comunicação da Anvisa, emissoras de TV anunciaram que vão transmitir a reunião. A data da reunião corresponde ao último dia do prazo definido para analisar pedidos de uso emergencial de vacinas.
A Anvisa é o órgão responsável pela liberação de imunizantes e medicamentos no Brasil. Serão analisados os dados de relatório elaborado pela área técnica do Instituto Butantan e da Fiocruz sobre os respectivos pedidos.
Feita a análise, a diretoria da agência definirá, por meio de votação, se libera ou não a aplicação das vacinas.
Caberá a cinco membros da Diretoria Colegiada da Anvisa a autorização de uso emergencial das vacinas: Antônio Barra Torres (diretor-presidente); Meiruze Sousa Freitas; Cristiane Rose Jourdan Gomes; Romison Rodrigues Mota; e Alex Machado Campos.
De acordo com os pleiteantes, foram entregues à Anvisa 100% dos documentos e dados exigidos no processo de avaliação. Nos últimos dias, a agência ainda cobrava a apresentação de informações pendentes.
Hoje, de acordo com o painel que monitora a análise das vacinas, 44,86% dos documentos da CoronaVac já haviam sido analisados, enquanto 55,14% estavam em análise. No caso da vacina de Oxford/AstraZeneca, 49,45% do processo estava concluído e 50,55% estava pendente.
O Ministério da Saúde vem afirmando que, caso a Anvisa venha a aprovar o uso emergencial das vacinas neste domingo, a imunização começaria já na próxima quarta-feira (20).
















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.