Anvisa nega pedido da Saúde para importação da vacina indiana Covaxin
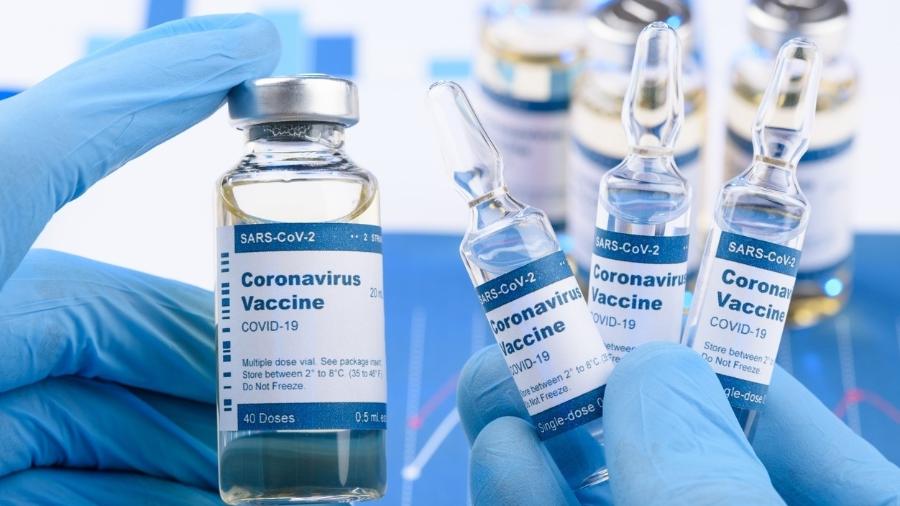
A Anvisa (Agência Nacional de Vigilância Sanitária) negou o pedido de importação e utilização excepcional da vacina Covaxin, produzida pelo laboratório indiano Bharat Biotech. O pleito do Ministério da Saúde, analisado hoje pela agência, dizia respeito à importação de 20 milhões de doses da Covaxin para o combate à pandemia da covid-19. A decisão foi por unanimidade, com um placar de 5 a 0.
Em seu voto, o relator do processo, diretor Alex Machado Campos, alegou a ausência de apresentação de documentos mínimos necessários para se avaliar o risco de uso da vacina indiana na população brasileira. "Estamos aqui no plano da incerteza", afirmou.
É uma rotina para a Anvisa deferir ou indeferir pedidos. Por trás está algo mais importante que é garantir a segurança da população."
Alex Machado Campos, diretor da Anvisa
Durante coletiva, a equipe técnica da Anvisa foi questionada sobre eventual recurso do ministério da Saúde para importação do lote de Covaxin. "O pedido já foi analisado à luz da lei, então um novo pedido seria avaliado de acordo com esta lei, sendo necessário cumprir os requisitos estabelecidos — isto é, apresentação dos documentos que faltaram e sanar questões de boas-práticas verificadas na inspeção", afirmou a gerente-geral de Inspeção e Fiscalização Sanitária, Carolina Marino.
Em audiência pública ocorrida na Câmara Federal durante a manhã, o ministro da Saúde, Marcelo Queiroga, afirmou, no entanto, que não descarta manter a compra dos imunizantes.
Riscos aos usuários
Também nesta semana, e em outro processo, a Anvisa negou a certificação de boas práticas à empresa fabricante da Covaxin. Esse processo foi rememorado pelo relator, que destacou, entre as inconformidades encontradas, riscos aos usuários por falta de comprovação de método para identificar a potência da vacina, isto é, a resposta imune contra a covid-19, comprometendo a sua eficácia.
A empresa também não conseguiu comprovar que adota todas as regras para esterilização do produto, outro ponto relacionado à segurança, bem como não teria mostrado, de acordo com a Anvisa, estratégias adequadas para garantir a pureza do produto.
Sobre a não cessão do certificado de boas práticas, o diretor-presidente Antônio Barra Torres afirmou, em entrevista ao Brasil Urgente, da TV Bandeirantes, após a reunião da Anvisa, que foram enviados cinco inspetores à Índia para visitar os locais de produção do insumo IFA e das vacinas já envasadas.
"O resultado dessa inspeção não nos permitiu entregar o certificado de boas práticas. Hoje tivemos a análise de um pedido de importação em caráter excepcional. Tanto um quanto outro não reuniram as condições mínimas para aprovação da Anvisa. É importante frisar que isso não é um fechamento de porta, não é o fim das tratativas com o fabricante", afirmou Barra Torres, acrescentando que, mediante as alterações e complementos necessários, uma nova análise poderá ser feita.
A diretora Meiruze Sousa destacou que a decisão de hoje é exclusiva quanto a esta ação. Ela alegou que o voto não coloca em dúvida a empresa, mas o lote de importação referente ao pedido. Deste modo, é possível que novos pedidos de autorização para importação e utilização sejam apresentados.
Não existe porta fechada para nenhuma vacina, mas no momento precisamos de apresentação de comprovação de boas práticas. Então neste sentido, no momento, eu acompanho o diretor relator no sentido de proteger a população brasileira."
Meiruze Sousa, diretora da Anvisa
Vacina da Janssen aprovada
Momentos antes, a Anvisa aprovou o uso emergencial da vacina da Janssen contra a covid-19 no Brasil. A aprovação do imunizante fabricado pela Johnson & Johnson foi unânime: quatro diretores e o presidente da agência votaram a favor do pedido.
O fármaco será importado ao custo de cerca de US$ 10 a dose — não há previsão de parcerias no Brasil para produção nacional. No país, só as vacinas da AstraZeneca/Oxford e da Pfizer já obtiveram o registro definitivo. A CoronaVac, a mais usada e em produção pelo Instituto Butantan, tem autorização de uso emergencial.
















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.