Anvisa recebe mais dados da Pfizer para analisar uso de vacina em crianças
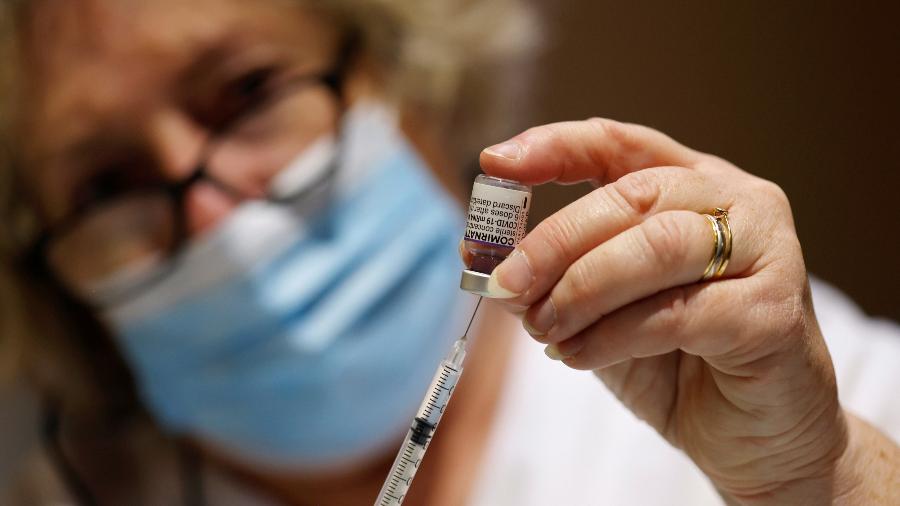
A Anvisa (Agência Nacional de Vigilância Sanitária) informou ontem que recebeu respostas da Pfizer sobre as exigências pedidas anteriormente pela agência para analisar o uso do imunizante do laboratório em crianças de 5 a 11 anos.
De acordo com a agência, que é vinculada ao Ministério da Saúde, os novos dados enviados pelo laboratório já estão sendo "verificados pela equipe técnica da Anvisa que já estava analisando os demais dados entregues anteriormente pelo laboratório".
No dia 12 de novembro, a Pfizer fez um pedido de liberação da vacinação de crianças entre cinco e 11 anos contra a covid-19 com o imunizante do laboratório.
Em 23 de novembro, a agência exigiu ao laboratório a apresentação de dados adicionais por enxergar "lacunas e dados importantes que precisavam ser incluídos no processo".
Em razão desta decisão, a Anvisa mudou os prazos para a divulgação do parecer da solicitação, que eram de 30 dias anteriormente. Os prazos estavam suspensos até que a Pfizer entregasse os dados solicitados pelo órgão.
Entre as informações pedidas pela agência reguladora no final do mês passado estavam questões relacionadas à eficácia, segurança da vacina e a resposta do imunizante contra a variante delta. (Veja lista completa abaixo)
De acordo com Cristiano Zerbini, coordenador de testes clínicos do laboratório Pfizer no Brasil, o estudo que serviu como base para o pedido observou que a proteção contra o coronavírus para as crianças de 5 a 11 anos, depois da 2ª dose, foi superior a 90%.
"É uma proteção muito boa e próxima do que conseguimos em adultos", disse Zerbini, na ocasião. "A segurança também foi bastante boa e muito semelhante ao que nós obtivemos em adolescentes de 12 a 16 anos", acrescentou.
Exigências feitas pela Anvisa à Pfizer
Veja abaixo às exigências da Anvisa para a Pfizer:
- dados de eficácia, dados de segurança da Coorte 2 e análises exploratórias de imunogenicidade contra a variante Delta, conforme enviado ao FDA/EUA;
- dados recentes de farmacovigilância (relatório de segurança mensal /Summary Monthly Safety Report (SMSR);
- discussão consubstanciada sobre o risco identificado miocardite/pericardite para crianças de 5 a <12 anos de idade, incluindo comparações (incluindo a incidência observada) com outras faixas etárias e por sexo;
- Informações quanto as diferenças entre as ações previstas no Plano de Minimização de Riscos e de farmacovigilância encaminhado à Anvisa em relação ao aprovado pela FDA/EUA;
- relatório de miocardite e pericardite, conforme compromisso com a FDA/EUA;
- envio de informações exigências e repostas às exigências encaminhadas pela FDA/EUA e Agência europeia de medicamentos (EMA).
















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.