Anvisa define regras para autorização temporária à vacina contra a covid-19
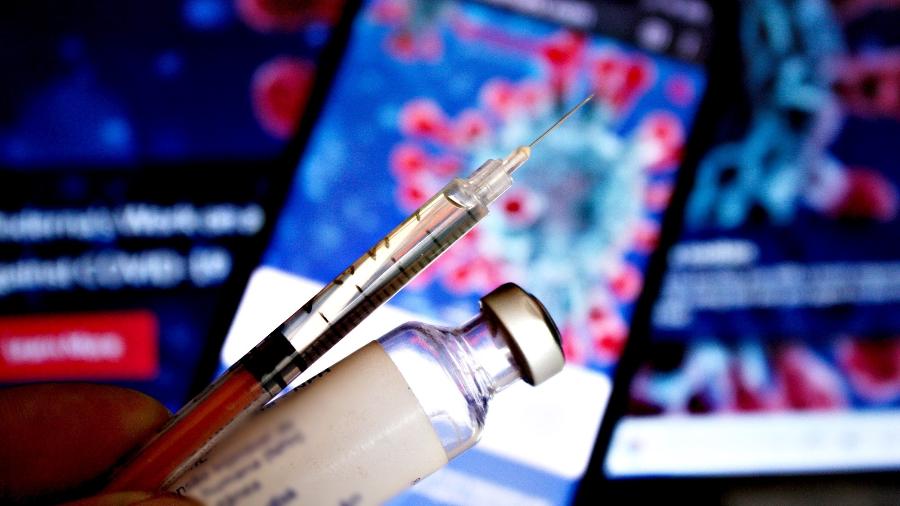
A Anvisa (Agência Nacional de Vigilância Sanitária) divulgou hoje um guia com requisitos para pedidos emergenciais de autorização para vacinas contra o coronavírus no país. O objetivo, segundo o órgão regulador, é orientar as empresas sobre as informações necessárias para facilitar esse aval para imunizantes experimentais.
Essa autorização é diferente do registro definitivo. Além de temporária, válida apenas enquanto a emergência de saúde pública estiver declarada, ela é destinada a uma parcela muito específica da população, podendo ser cancelada a qualquer momento. O aval também não permite a vacinação em massa, nem a comercialização de imunizantes.
"A autorização de uso emergencial não implica, de nenhuma maneira, em diminuição dos critérios e do rigor de qualidade, segurança e eficácia necessários. Ainda existem dados a serem gerados, ainda existem informações a serem compiladas. Mas se o risco/benefício está bem estabelecido, é possível que concedamos autorização para uso em caráter de emergência", explicou Gustavo Mendes, gerente-geral de Medicamentos e Produtos Biológicos da Anvisa, durante coletiva.
Para tanto, serão feitas análises independentes de cada vacina e, no final, a decisão ficará a cargo da Diretoria Colegiada da Agência. Serão analisados estudos não clínicos e clínicos feitos em humanos e dados relativos à qualidade, boas práticas de fabricação, estratégias de monitoramento e controle, além de quaisquer outras evidências científicas.
O uso emergencial será liberado apenas para o público testado previamente nos estudos. O restante da população só terá acesso à vacina quando houver o registro sanitário definitivo no Brasil.
Pode fazer fazer o pedido a empresa desenvolvedora da vacina que tenha AFE (Autorização de Funcionamento de Empresa) emitida pela Anvisa, com atividade específica para fabricar ou importar medicamentos. Também devem ser apresentadas informações que garantam a qualidade da vacina, a fabricação e sua conservação.
Por ora, de acordo com a Anvisa, nenhuma empresa protocolou pedidos de autorização para uso emergencial de vacinas.
Além desse processo, com o andamento e condução do ensaio clínico na fase 3 em andamento, é preciso que a vacina venha com um DDCM (Dossiê de Desenvolvimento Clínico de Medicamento) autorizado pela agência.
Profissionais de saúde e idosos terão prioridade
Uma versão preliminar do plano nacional de imunização contra a covid-19 foi divulgada ontem pelo secretário de Vigilância em Saúde, Arnaldo de Medeiros. Serão quatro fases, priorizando profissionais da saúde, idosos, indígenas, professores, forças de segurança e presos, normalmente mais vulneráveis e expostos à doença.
"É extremamente importante avisarmos à população brasileira que o Ministério da Saúde, através do Plano Nacional de Imunizações [PNI], não descarta nenhuma vacina. O que nós queremos é uma vacina que seja registrada na Anvisa [Agência Nacional de Vigilância Sanitária] e que mostre eficácia e segurança", acrescentou Medeiros.
Os trabalhadores da saúde devem ser os primeiros a ser vacinados, seguidos pelos idosos acima de 75 anos ou a partir de 60 anos que vivem em asilos e instituições psiquiátricas. Depois, na terceira fase, vem a população indígena e, na quarta, os professores, as forças de segurança e os presos.
A expectativa é começar a vacinar a população, seguindo a ordem de prioridade, a partir do primeiro trimestre de 2021. Pelas contas do Ministério da Saúde, as quatro fases da campanha abrangem 109,5 milhões de pessoas imunizadas, em duas doses.















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.