Senado aprova MP que agiliza aprovação de vacinas para uso emergencial
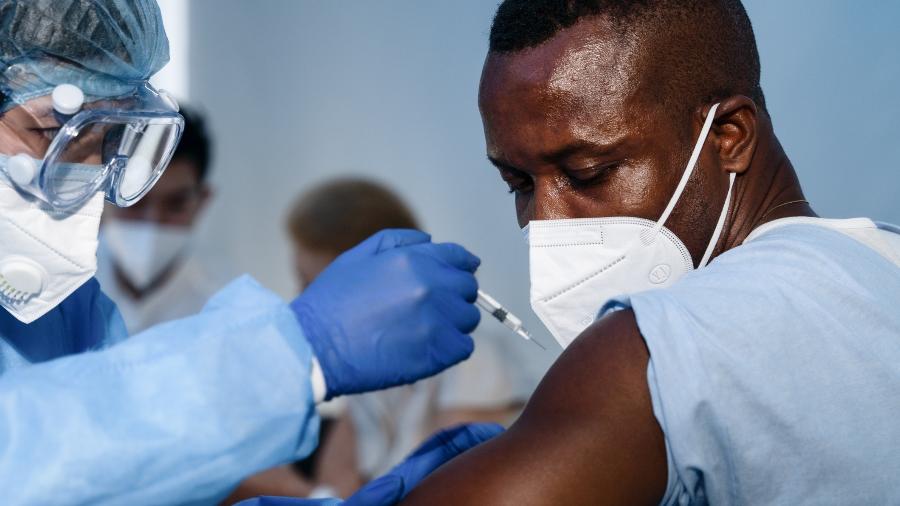
O Senado Federal aprovou hoje a MP (Medida Provisória) 1003/2020, que agiliza a autorização temporária de vacinas pela Anvisa (Agência Nacional de Vigilância Sanitária) para uso emergencial no Brasil e autoriza o país a participar do Covax Facility, o consórcio para acesso global de vacinas contra o coronavírus.
O texto prevê a liberação em até cinco dias para vacinas que já tenham autorização para uso emergencial em determinados países, critério que atualmente não é levado em conta pela Anvisa. A agência brasileira hoje prevê prazo de até dez dias para analisar o uso emergencial de imunizantes com estudos de fase 3 realizados no Brasil e de até 30 dias para aqueles que só foram testados no exterior, segundo nova regra anunciada ontem pela Anvisa.
"Essa autorização temporária observará as mesmas condições do registro e da autorização de uso concedidos pela autoridade sanitária estrangeira, devendo o fabricante comprometer-se a concluir os estudos clínicos em curso, e será válida enquanto perdurar a emergência em saúde pública decorrente da covid-19", diz a MP.
Como inclui a agência reguladora russa, a medida deve facilitar a importação e liberação para uso emergencial da vacina Sputnik V, desenvolvida pelo Instituto Gamaleya. Países vizinhos como Argentina, Paraguai e Bolívia, por exemplo, já começaram a aplicar o imunizante.
Pouco antes do anúncio da aprovação da medida, o diretor-presidente da Anvisa, Antônio Barra Torres, disse que a agência direcionaria todos os esforços para buscar cumprir o novo prazo, se assim aprovado pelo Legislativo — como, de fato, aconteceu.
"A Anvisa continuará fazendo seu trabalho, continuará trabalhando para fornecer respostas para a sociedade sem abrir mão de nenhum milímetro da segurança, porque quem está lá na ponta é o povo brasileiro", declarou ele durante transmissão ao vivo ao lado do presidente Jair Bolsonaro (sem partido).
O texto aprovado pelo Senado excluiu, porém, o termo de consentimento ou de responsabilidade que seria exigido a quem se vacinasse contra a covid-19. Sua adoção havia sido defendida por Bolsonaro, que chegou a dizer que cidadãos que desejam se imunizar deveriam se responsabilizar por eventuais efeitos colaterais.
Na justificativa, parlamentares afirmaram que a responsabilidade por garantir a qualidade é da Anvisa.
Covax Facility
O Covax Facility é organizado pela OMS (Organização Mundial da Saúde) e integra mais de 170 países. Como participante, o Brasil deve receber a quantidade de doses para imunizar 20% da população.
A medida entrou na Câmara dos Deputados em setembro de 2020 e, em novembro, já estava em caráter de emergência no Senado.
Ainda no ano passado, o Brasil chegou a ofertar R$ 2,5 bilhões para a organização. Ontem, a CEPI (Coalizão para Inovações em Preparação para Epidemias) e Aliança Gavi anunciaram que o Brasil vai receber 10,6 milhões de doses da vacina AstraZeneca/Oxford ainda neste semestre.
Segundo o relator da medida, senador Confúcio Moura (MDB-RO), uma das emendas da proposta garante que todos os países sejam beneficiados da mesma forma. Para ele, a participação irá "assegurar o número de vacinas para toda a população brasileira", possibilitando ainda a "ampla gama" da imunização e a negociação dos preços.
"Este é um pedido de autorização ao Poder Executivo que o Congresso Nacional quer para autorizar o governo federal, o Brasil, a participar de um consórcio internacional", defendeu.
Aprovada pelo Senado de forma simbólica, a matéria segue para sanção do presidente Jair Bolsonaro.
















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.