Anvisa aprova uso emergencial de medicamento contra covid-19
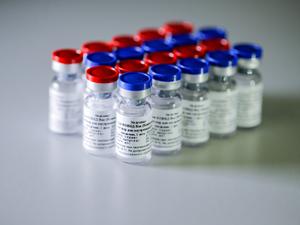
A Anvisa (Agência Nacional de Vigilância Sanitária) aprovou hoje, por unanimidade, o pedido de uso emergencial de um medicamento contra a covid-19 que é resultado da combinação dos anticorpos monoclonais casirivimabe e imdevimabe. O coquetel, chamado de Regen-Cov, não previne a doença, mas apresentou resultados positivos para evitar o agravamento do quadro em pacientes com fatores de risco.
Segundo a Anvisa, "a indicação dos medicamentos é para quadros leves e moderados da doença, em adultos e pacientes pediátricos (12 anos ou mais) com infeção por Sars-CoV-2 confirmada por laboratório, e que possuem alto risco de progredir para formas graves da doença".
Os fatores de risco considerados para a indicação do medicamento são: idade avançada (65 anos ou mais), obesidade, doença cardiovascular, hipertensão, doença pulmonar crônica, asma, diabete, doenças renais crônicas, incluindo pacientes em diálise, imunossuprimidos e doenças hepáticas crônicas.
A Anvisa liberou o uso do remédio apenas em ambiente hospitalar — não haverá comercialização em farmácias —, sendo que não está autorizado o uso em pacientes já internados ou que necessitam de oxigênio de alto fluxo ou ventilação mecânica em seus tratamentos.
De acordo com dados do estudo clínico, os anticorpos não demonstraram benefício em pacientes internados, podendo até estar associados a desfechos clínicos piores quando usados.
Anvisa
Ainda segundo a Anvisa, o casirivimabe e o imdevimabe devem ser administrados juntos por infusão intravenosa (IV) e os possíveis efeitos colaterais incluem anafilaxia (reação alérgica aguda), febre, calafrios, urticária, coceira e rubor. "A segurança e a eficácia dos anticorpos continuam a ser avaliadas por meio de estudos que estão em andamento", diz a nota.
O coquetel de casirivimabe e imdevimabe está liberado para uso em caráter emergencial nos Estados Unidos desde novembro passado para pacientes com ao menos 12 anos e 40kg, tendo sido utilizado no tratamento do então presidente Donald Trump.
Anticorpos monoclonais são proteínas feitas em laboratório e que imitam a capacidade do sistema imunológico de combater patógenos nocivos, como vírus. O casirivimabe e o imdevimabe são anticorpos monoclonais que são especificamente direcionados contra a proteína de pico (spike) de Sars-CoV-2, projetada para bloquear a adesão e a entrada do vírus em células humanas.
Esse não é o único coquetel que está em fase de análise pela Anvisa. A agência analisa desde 30 de março o pedido de uso emergencial de medicamento para tratar covid da empresa Eli Lilly do Brasil Ltda. O coquetel tem função semelhante e é uma combinação dos medicamentos biológicos banlanivimabe e etesevimabe.
Em março, a Anvisa aprovou o uso do rendesivir, da farmacêutica Gilead, contra a covid-19, o primeiro registro para um medicamento com uso indicado em bula para tratamento da doença.
Preço pode limitar uso pelo SUS, diz pesquisador
O infectologista e pesquisador da Fiocruz Júlio Croda afirmou que, apesar dos bons resultados do medicament,o teme que ele tenha um "uso limitado" na rede pública de saúde devido ao custo.
"Ele reduziu a carga viral em pacientes que não tinham tido a doença, reduziu a hospitalização em torno de 70%, entretanto, tem um custo elevado. A dose desse tratamento sai entre US$ 1200 e US$ 1500. Como um tratamento para evitar casos graves, continua sendo caro, e dificilmente isso vai chegar aos pacientes do SUS e nem a fabricante tem condições de produzir ampolas suficientes", afirmou o infectologista em entrevista à CNN Brasil.
Questionado sobre a eficácia do medicamento contra as variantes do novo coronavírus, o pesquisador disse que ainda não há "dados de ensaios clínicos em relação a isso. O que há são dados in vitro de que ele neutraliza a nossa variante P1".
Estudos
O Regen-Cov é elaborado pela empresa americana Regeneron Pharmaceuticals em parceria com a farmacêutica suíça Roche. O gerente-geral de medicamentos da Anvisa, Gustavo Mendes, afirmou que seu uso "reduziu significativamente o número de hospitalização e morte em paciente laboratorial sintomático com um ou mais fator de risco para doença grave."
No caso da autorização no Brasil, a dose é de 600 mg de cada um dos dois medicamentos, que devem ser administrados juntos e por meio de infusão intravenosa única (por meio de uma bolsa, semelhante à administração de um soro, por exemplo). A posologia é, portanto, distinta da autorizada nos Estados Unidos e na Europa, que prevê o 1,2 mil mg. Segundo Mendes, a empresa submeteu a nova posologia nos locais citados.
O gerente-geral de medicamentos destacou que o tratamento passou por quatro estudos não clínicos distintos, nos quais não foram identificadas "questões maiores" em relação à segurança, considerada com perfil "aceitável". "Os ensaios realizados não geraram preocupação que ensejasse uma investigação específica", apontou.
O benefício seria perceptível a partir do segundo dia após a aplicação. Segundo o estudo considerado pela Anvisa, houve redução de 70,4% no número de pacientes hospitalizados por covid-19 — quando comparado ao grupo que recebeu placebo.
Nesse estudo, os eventos adversos graves foram mais frequentes no grupo placebo. Ao todo, 0,3% do total que recebeu o tratamento teve uma reação de hipersensibilidade. No caso das doses de 2,4 mil mg, a redução foi semelhante, de 71,3%, destacou Gustavo Mendes.
O medicamento tem validade de 12 meses quando armazenado de 2ºC a 8ºC. Quando diluído, pode ser armazenado por até quatro horas em temperatura ambiente e, se refrigerado, por até 36 horas.
Com informações das agências Reuters e Estadão Conteúdo















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.