Após anúncio de Doria, Anvisa diz que faltam etapas para liberar CoronaVac
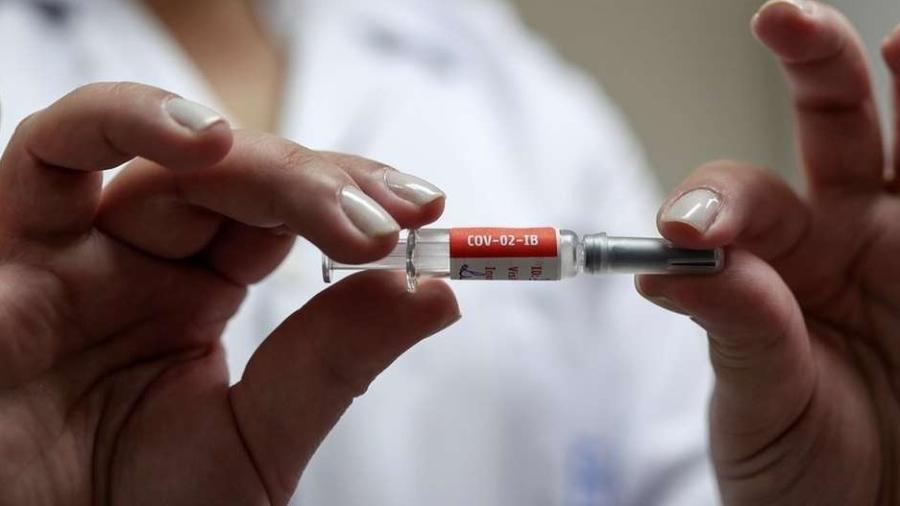
Após anúncio feito pelo governador de São Paulo, João Doria (PSDB), sobre o plano estadual de vacinação contra a covid-19, a Anvisa (Agência Nacional de Vigilância Sanitária) reagiu, em nota, dizendo que faltam etapas para liberar a CoronaVac —vacina desenvolvida pela farmacêutica chinesa Sinovac em parceria com o Instituto Butantan.
O Butantan já havia dito, mais cedo, que deve encaminhar os dados de estudos que comprovem a segurança e a eficácia da vacina na semana que vem. E que a previsão de início da vacinação conta com "intercorrências" que podem acontecer em meio ao processo de registro do imunizante.
Na nota, a Anvisa afirmou que, além dos estudos de eficácia, precisa enviar um documento sobre a inspeção feita no laboratório Sinovac, na China, que terá de ser respondido pelo Butantan. Depois, será produzido um relatório de inspeção, que é o documento que aprova ou não a vacina. A expectativa da agência regulatória é que todo o processo fique pronto entre 30 de dezembro de 2020 e 11 de janeiro de 2021.
Pelo calendário anunciado por Doria, o primeiro grupo a ser vacinado (profissionais da saúde, indígenas e quilombolas) receberá a primeira dose a partir de 25 de janeiro de 2021, caso ocorra a liberação da Anvisa.
Em entrevista antes de divulgar a nota, o diretor-presidente da Anvisa, Antônio Barra Torres, desejou "boa sorte" a autoridades que estipulam prazos para o início da vacinação, sem citar o nome de Doria. Mas afirmou que a agência precisa de "no mínimo 60 dias" para analisar os documentos. (leia mais abaixo)
O que falta?
De acordo com a Anvisa, o Instituto Butantan já encaminhou dois estudos (o primeiro em 2 de outubro e o segundo, que ainda está em análise, em 30 de novembro), mas faltam também dados da fase 3 —que foi encerrada há cerca de duas semanas. (Veja a nota, na íntegra, abaixo)
"Não foram encaminhados dados relativos à fase III, que é a fase que confirma a segurança e eficácia da vacina. Esse dado é essencial para a avaliação tanto de pedidos autorização de uso emergencial quanto pedidos de registro", afirmou a Anvisa.
Veja abaixo a nota da Anvisa:
Esclarecimentos sobre análise dos estudos da vacina Sinovac.
1. Até o momento, foram encaminhados dois conjuntos de dados de estudos de segurança e eficácia por meio do procedimento de submissão contínua. O primeiro foi encaminhado em 02/10/2020 e sua análise já foi concluída. O segundo foi encaminhado em 30/11/2020 e está em análise.
2. Não foram encaminhados dados relativos à fase III, que é a fase que confirma a segurança e eficácia da vacina. Esse dado é essencial para a avaliação tanto de pedidos autorização de uso emergencial quanto pedidos de registro.
3. A inspeção na empresa Sinovac foi concluída no dia 04/12: Após o final da inspeção, a equipe inspetora elabora um documento (Anexo III do POP-O-SNVS-001), onde são listados todas os achados da inspeção (potenciais não conformidades). Este documento será formalmente enviado ao Instituto Butantan até 3 dias úteis após a inspeção. O documento deve ser respondido formalmente pelo Instituto Butantan em até 5 dias úteis após o seu recebimento. Com base nas respostas fornecidas pelo IB, a equipe inspetora elabora o Relatório de Inspeção, o qual apesar de ter prazo procedimental máximo de 31 dias úteis, foi planejado nesta missão para que leve 10 dias úteis no máximo. O Relatório de Inspeção é o documento conclusivo quanto à Certificação, podendo as conclusões deste levarem ao deferimento ou indeferimento da certificação. Somando-se os dias apresentados, conclui-se que o Relatório de Inspeção deverá ser finalizado entre 30 de dezembro a 11 de Janeiro de 2020.
4. É importante destacar que para a solicitação de Autorização de Uso Emergencial é esperado que sejam apresentados minimamente os dados descritos do Guia sobre os requisitos mínimos para submissão de solicitação de autorização temporária de uso emergencial, em caráter experimental, de vacinas covid-19.
1ª fase da vacinação terá 18 milhões de doses
Mesmo sem ter autorização do uso da CoronaVac, o governo paulista já firmou um acordo para ter 46 milhões de doses do imunizante —o que é suficiente para vacinar 23 milhões de pessoas, já que são necessárias duas doses. O tempo previsto entre a primeira e a segunda dose é de 21 dias.
A primeira fase da vacinação, anunciada hoje, deve contar com 18 milhões de doses (ou seja, para 9 milhões de pessoas).
Em coletiva no Palácio dos Bandeirantes, o governador também informou oferecerá 4 milhões de doses a outros estados, para que eles vacinem profissionais de saúde —a quantidade suficiente para vacinar 2 milhões de pessoas, já que serão necessárias duas doses por pessoa. Ele, porém, não revelou quais governadores solicitaram a vacina a seus estados —citou apenas dois prefeitos.
"No estado de São Paulo, a vacinação está programada para começar no dia 25 de janeiro. A fase 1 será destinada para profissionais de saúde e pessoas com mais de 60 anos. A escolha do público-alvo levou em conta a incidência de óbitos, um total de 77% das mortes por covid foi concentrado nas pessoas acima de 60 anos", afirmou Doria.
O governador disse que os recursos para a campanha de vacinação sairão do "Tesouro do estado", mas não deu detalhes. "[A vacina] será gratuita para todos", disse.
Processo de aprovação e registro é dinâmico, diz diretor
Quatro vacinas contra a covid estão em teste no Brasil. Horas depois da coletiva, em entrevista à rádio Jovem Pan, o diretor-presidente da Anvisa disse que ainda "não tem os protocolos" a serem analisados para aprovação da CoronaVac.
"Antes de verificarmos estes protocolos de registro, precisamos acessar os documentos dos estudos clínicos referentes à fase 3 dos testes. No entanto, estes estudos ainda não se encerraram. Para efetuarmos o registro de vacina contra o coronavírus, demandamos no mínimo 60 dias para analisarmos os documentos", disse Barra Torres.
"Apesar da previsão, não vou criar expectativa na população que já está tão sofrida com a pandemia com as notícias conflitantes. É terrível criar uma expectativa que pode não se concretizar. Preciso deixar claro que o processo de aprovação e registro dos imunizantes são dinâmicos, ou seja, podem ocorrer interferências e problemas capazes de mudar todo o calendário. Poderemos ter a grata alegria de, logo na virada do ano, termos uma possibilidade concreta de distribuição da vacina ou de, ainda em 2020, aprovarmos o uso emergencial. Essas hipóteses podem acontecer, mas não devemos colocar prazos", afirmou.
Butantan deve entregar documentos semana que vem
Na coletiva, o Instituto Butantan disse os documentos com a última fase de testes serão enviados à Anvisa na semana que vem, no dia 15 de dezembro. Esses documentos incluem, em especial, o resultado do teste da eficácia. Autoridades de saúde admitem que não há garantia de que a vacina será aprovada, mas se mostraram confiantes.
Segundo Dimas Covas, diretor do Instituto Butantan, o planejamento para o dia 25 inclui possíveis intercorrências com a agência. Originalmente, Doria tinha anunciado o início da imunização para dezembro.
"A alteração de 15 [de dezembro] a 25 [de janeiro] é porque a realidade impôs. Estamos no processo da produção da vacina e no procedimento de termina avaliação de eficácia do estudo clínico, bem como [a avaliação pelo órgão] da fábrica lá na China. São esses três elementos que vão compor registro. Essa data é compatível com esses três elementos. É uma data inicial e com grande probabilidade acontecer conforme previsto", afirmou Covas, na coletiva.















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.