Saúde rebate Pfizer e compara exigências da Anvisa às da FDA, dos EUA
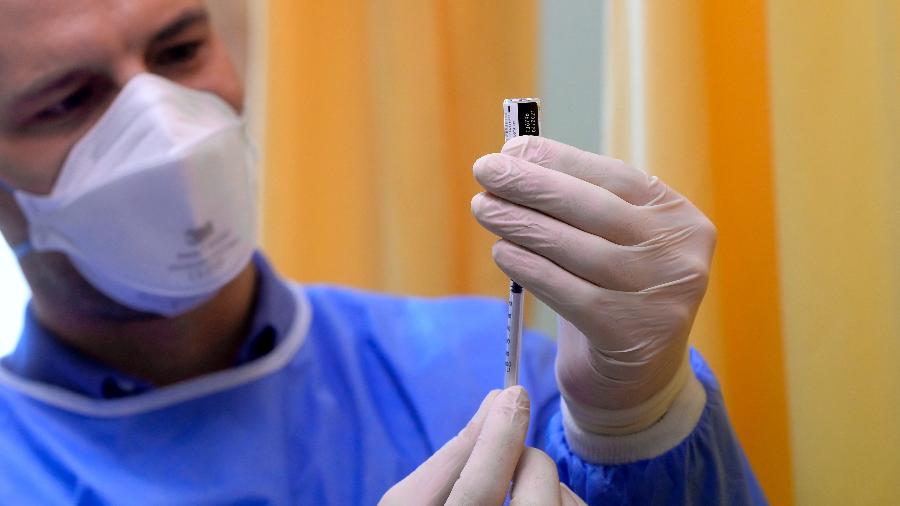
O secretário-executivo do Ministério da Saúde, Elcio Franco, rebateu hoje a argumentação da farmacêutica americana Pfizer sobre as exigências da Anvisa (Agência Nacional de Vigilância Sanitária) para aprovação do uso emergencial da vacina contra a covid-19.
Segundo o secretário, a FDA (Food and Drug Administration), agência federal do departamento de Saúde e Serviços Humanos dos Estados Unidos, tem as mesmas exigências que a Anvisa com relação à autorização para uso emergencial.
"Nos causou espécie o pronunciamento ao esclarecer que estava com dificuldade pelas solicitações da Anvisa, uma vez que os aspectos são os mesmos que o da FDA para uso emergencial", disse, em coletiva de imprensa.
"Causou espécie porque esses laboratórios já têm autorização pela FDA e de outras agências pelo mundo. Vamos buscar maior diálogo com o laboratório. Temos incentivado porque na solicitação para uso emergencial ela é designada para grupos específicos."
Elcio Franco também afirmou não saber qual foi o motivo da eventual dificuldade da Pfizer para a submissão da sua vacina contra a covid-19 em uso emergencial e disse que o tema cabe ao laboratório com a Anvisa.
Segundo ele, questionamento sobre essa dificuldade tem de ser dirigida à Pfizer, não ao Ministério da Saúde ou à Anvisa. "Não sei se faltou uma folha, um documento, uma planilha, um relatório. Que tipo de documento está faltando. Isso a Anvisa nem no seu site ela divulga", disse.
Franco acrescentou que, por isso, não é possível estimar quando a autorização será concedida.
Ao ser indagado se o ministério poderia interferir nessa negociação, uma vez que a vacina da Pfizer é vista como a possibilidade de o Brasil contar com um imunizante no futuro próximo, o secretário-executivo avaliou que não será necessariamente a primeira vacina no país, porque, se a Pfizer não quiser se submeter às regras da Anvisa, "não posso pegar a Pfizer pelo braço, levar lá e falar 'Pfizer, entregue seu relatório para a Anvisa'".
Ele ressaltou que a Anvisa é a responsável por assegurar à população uma vacina segura e eficaz.
O secretário-executivo da pasta, Elcio Franco, reforçou que o ministério pretende, "na melhor hipótese", começar a vacinação em 20 de janeiro de 2021. Num prazo mais longo, a partir de 10 de fevereiro. A data depende de uma série de fatores, como autorizações pela Anvisa, logística e fornecimento das doses por parte dos fabricantes, afirmou.
5,8 milhões de doses de cloroquina distribuídas
Ontem, o presidente Jair Bolsonaro (sem partido) usou dados imprecisos ou sem comprovação científica para defender que "não errou [em] nenhuma" medida tomada contra a pandemia. Ele também voltou a dizer que "não precisa ficar com pavor" do coronavírus e que não vai se vacinar quando um imunizante estiver disponível no Brasil.
Franco afirmou que o ministério teve dotação de R$ 198,1 bilhões em 2020 — R$ 133,9 bilhões previstos na Lei Orçamentária Anual mais R$ 64,2 bilhões de créditos extraordinários para o combate à covid-19. Ele citou ações da pasta para a disponibilidade de leitos de UTI (Unidade de Terapia Intensiva) e equipamentos, além da compra de medicamentos para intubação.
O secretário-executivo disse que foram distribuídos, até o momento, 5,8 milhões de unidades de cloroquina e 302 mil unidades de hidroxicloroquina de acordo com demandas dos estados. Nenhum dos dois remédios têm efeito comprovado contra a covid-19.
Também foram distribuídos 21 milhões de unidades de Oseltamivir, voltado ao combate da gripe H1N1.
Pfizer cita que esbarrou em "dificuldades"
Ontem, a Pfizer informou que não irá submeter a sua vacina, produzida em parceria com a BionTech, para o uso emergencial no Brasil e deve se apoiar na chamada submissão contínua.
Em comunicado, a farmacêutica explicou que teve uma reunião com representantes da Anvisa para esclarecer dúvidas sobre o processo de submissão, mas que acabou se esbarrando em dificuldades do Guia de Submissão para Uso Emergencial, elaborado pela própria agência brasileira.
A submissão contínua ainda não é o pedido de registro da vacina, mas sim uma forma de acelerar a análise dos dados por parte da Anvisa. Neste procedimento, os resultados das fases dos testes clínicos vão sendo apresentados à medida que ficam prontos, e não somente ao final da pesquisa.
O Brasil conta com mais de 7,5 milhões de casos confirmados de covid-19. Desde o começo da pandemia, 192.681 pessoas morreram devido à doença no país, segundo dados do Ministério da Saúde.
















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.