Anvisa recebe pedido de uso emergencial da vacina da CanSino contra covid
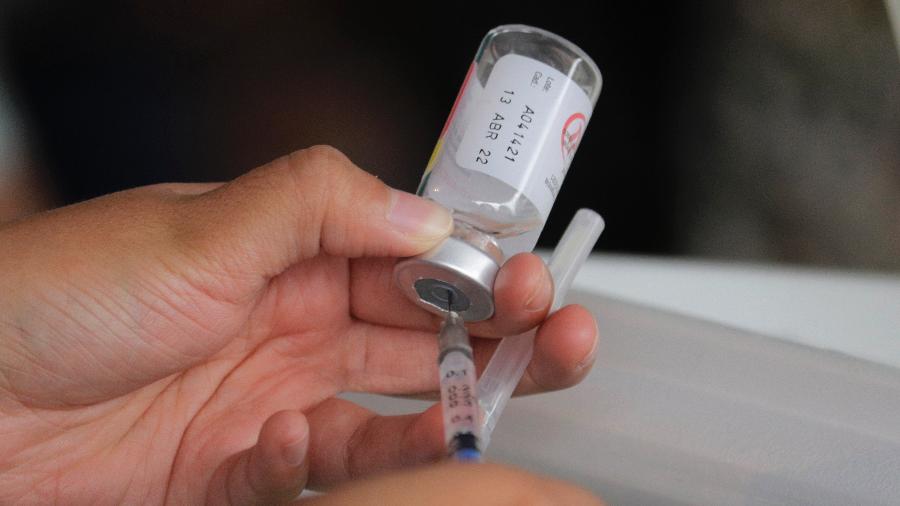
A Anvisa (Agência Nacional de Vigilância Sanitária) recebeu hoje o pedido de autorização para uso emergencial da vacina contra covid-19 produzida pelo laboratório CanSino, chamada Convidencia. O imunizante é de dose única.
A agência tem até sete dias úteis para analisar os documentos enviados pelo laboratório Biomm, representante do fabricante chinês no Brasil. O prazo, no entanto, não considera o tempo de resposta do laboratório, caso seja preciso responder questões técnicas feitas pela Anvisa no período.
"Nos pedidos de uso emergencial, as primeiras 24 horas são dedicadas a uma triagem do processo para verificar se os documentos necessários estão disponíveis. Se houver informações importantes faltando, a Agência pode solicitar as informações adicionais ao laboratório", explica a Anvisa.
Em maio deste ano, a agência já havia recebido o pedido por outra empresa, a Belcher Farmacêutica. Em junho, a Anvisa recusou o pedido devido ao "comprometimento de mecanismos" e ao rompimento da relação comercial entre o laboratório chinês e a Belcher Farmacêutica e o Instituto Vital Brazil.
















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.