Vacinas para crianças só devem chegar em fevereiro, avalia sociedade médica
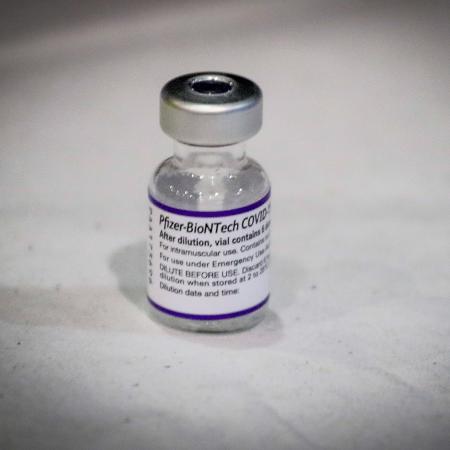
O presidente da SBIm (Sociedade Brasileira de Imunizações), Juarez Cunha, defendeu hoje que o Ministério da Saúde inicie rapidamente as tratativas com a Pfizer para aquisição da vacina contra a covid-19 para crianças de 5 a 11 anos. Já que se trata de um imunizante com composição diferente do indicado para adultos e como o país ainda não recebeu nenhuma dose, ele diz não acreditar que a vacinação comece nas próximas semanas.
"Temos que lembrar que é uma vacina diferente e, se essa decisão do ministério [de comprar] for tomada, essas vacinas só deverão estar disponíveis entre fevereiro ou março. Antes disso, não acho que tenha aqui no Brasil", diz.
A Anvisa (Agência Nacional de Vigilância Sanitária) aprovou ontem o uso emergencial da vacina da Pfizer para crianças de 5 a 11 anos no Brasil, mas a decisão de comprar ou não as doses é do Ministério da Saúde. A pasta foi questionada pelo UOL na manhã de ontem, mas até o momento não respondeu nem fez qualquer manifestação em redes sociais sobre a inclusão ou não da nova faixa etária no PNI (Programa Nacional de Imunização).
A aprovação foi muito comemorada por especialistas, que veem necessidade de correr contra o tempo para iniciar a vacinação devido à chegada da variante ômicron e à volta às aulas, em fevereiro.
Juarez Cunha afirma que, diante da falta do imunizante em solo nacional, o tema será debatido na câmara técnica --órgão que aconselha o ministério nas decisões sobre imunização. "O importante é que comece logo esse debate para que, quando pudermos ter a vacina, o ministério já tenha uma definição e possa distribuir de imediato", diz.
A pasta já tem um contrato assinado com o laboratório para compra de 100 milhões de doses da Pfizer em 2022, em que prevê a possibilidade de algumas dessas vacinas serem do composto para crianças.
Mas, em meio o silêncio do ministério, Cunha se coloca com o pé atrás.
A gente gostaria que o ministério se posicionasse da mesma forma que a gente e dizer que foi uma ótima notícia. Mas nós tivemos a mesma situação com a vacinação dos adolescentes. Quando a gente começou a defender, teve uma dificuldade de isso ser assimilado pelo ministério --inclusive com posições contrárias do presidente. Não é uma novidade que esteja acontecendo agora."
Juarez Cunha, presidente da SBIm
Sem interferência política
O presidente da SBIm também comentou a informação de que o presidente Jair Bolsonaro (PL) teria ficado furioso com a aprovação da Anvisa. Cunha se mostrou temeroso de que a posição pessoal do chefe do Executivo atrapalhe o processo de imunização.
"A gente sabe que a desinformação e as fake news atrapalham nosso processo vacinal. Se realmente a postura do presidente for essa [de se enfurecer com a aprovação da Anvisa], pode atrapalhar. Vamos ver os próximos capítulos e saber se essa vai ser a posição dele, se vai interferir na decisão científica --tanto da Anvisa, como das sociedades médicas. Esperamos que a política não interfira", diz.
A decisão da Anvisa foi tomada em comum acordo com todas as sociedades científicas brasileiras, entre elas a SBIm.
Segundo Cunha, a aprovação, porém, é apenas um "primeiro passo" para que a vacina da Pfizer seja incluída no PNI. Como ocorre com todos os assuntos da imunização, o tema será debatido na reunião na Câmara Temática de Imunizações do Ministério da Saúde, que é composta por especialistas, representantes dos governos estaduais e municipais e representantes de entidades científicas.
"Essas reuniões ocorrem às sextas-feiras, mas a pauta de amanhã não incluiu o tema porque foi fechada antes. Mas, em geral, o que é discutido nessa câmara é levado em consideração pelo PNI. Algumas situações acabam tendo mais dificuldade na decisão, como foi o caso do intervalo da dose de reforço", pontua.
Mas a posição da Anvisa e das sociedades científicas já é bem clara e conhecida: vacinas licenciadas são seguras e, sem nenhuma dúvida, beneficiam a coletividade. A eficácia e segurança dessa da Pfizer já estão provadas não só pelos dados apresentados hoje, mas pela experiência mundial."
Juarez Cunha, presidente da SBIm
Ceará abre cadastro infantil
Hoje, autoridades municipais e estaduais usaram suas redes sociais para comemorar a decisão da Anvisa e avisar que já estão com redes de saúde prontas para iniciar o processo, aguardando apenas a chegada do imunizante. O governo do Ceará, inclusive, abriu o cadastro para que os pais possam dar os nomes dos filhos para a lista de futura vacinação.
O Conass (Conselho Nacional de Secretários de Saúde) comemorou, em nota, a decisão da Anvisa e disse que "aguarda posicionamento do Ministério da Saúde quanto à sua aquisição, o que é de sua competência".
É importante destacar o alerta da Organização Mundial da Saúde (OMS) que aponta que o público entre 5 e 14 anos é o mais afetado pela nova onda de covid-19 na Europa e, apesar do menor risco em relação a outras faixas etárias, nenhuma outra doença imunoprevenível causou tantos óbitos em crianças e adolescentes no Brasil em 2021 como a covid-19."
Conass, em nota
Ainda afirma que aguarda "também com expectativa" a avaliação pela Anvisa da vacina CoronaVac, que teve pedido similar de uso emergencial pelo Instituto Butantan para a vacinação de crianças e adolescentes de 3 a 17 anos.
"Ela já amplamente utilizada em outros países, com disponibilidade imediata no Brasil e desenvolvida em plataforma conhecida, segura, eficaz e que permite a execução ordinária das demais vacinas do PNI", explica.

















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.