Anvisa recebe pedido de registro da vacina da CanSino contra a covid-19
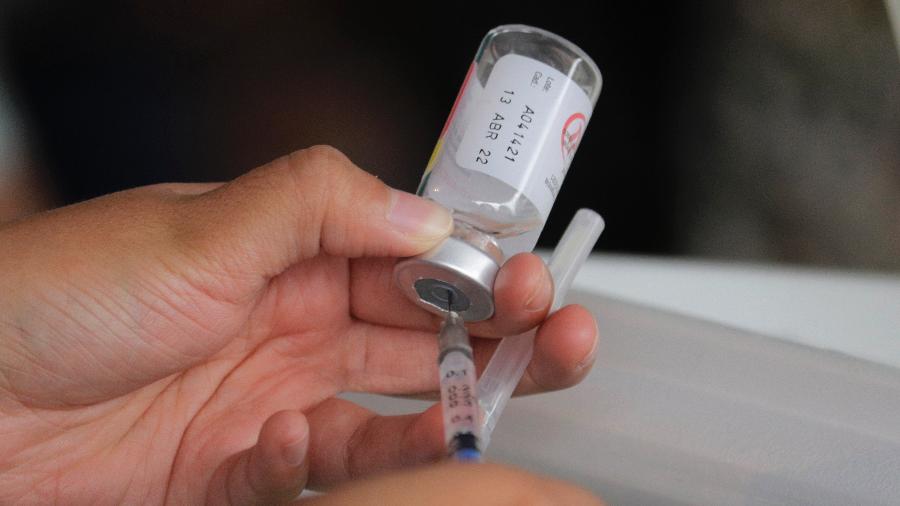
A Anvisa (Agência Nacional de Vigilância Sanitária) informou hoje ter recebido o pedido de registro de mais uma vacina contra a covid-19. O imunizante Convidecia teve a solicitação realizada pela farmacêutica Biomm S.A, responsável nacionalmente por representar a fabricante da vacina, a CanSino Biologicals, no Brasil.
Segundo a agência regulatória, a vacina da CanSino — que fez o pedido apenas para a aplicação em adultos — usa a tecnologia de adenovírus vetor, modo já utilizado em outras vacinas no Brasil.
A agência esclareceu que o protocolo do pedido foi recebido na hoje e já seguiu para a avaliação das áreas técnicas responsáveis. Agora, a CanSino Biologicals precisa aguardar até 60 dias para receber o parecer da Anvisa.
"A solicitação foi apresentada à Anvisa no âmbito da Resolução da Diretoria Colegiada (RDC) 415/2020, que contém critérios e procedimentos extraordinários para pedidos de registro decorrentes do novo coronavírus. A norma prevê, por exemplo, a análise prioritária e a possibilidade de se firmar termos de compromisso, como foi feito com outras vacinas contra a Covid-19 já autorizadas no Brasil", esclareceu a Anvisa.
A análise do imunizante fica por conta de três áreas diferentes da agência responsáveis por avaliar o pedido conjuntamente São elas: "a área de medicamentos, que avalia os aspectos e segurança e eficácia; a área de farmacovigilância, responsável pelo monitoramento e planos de acompanhamento da vacina após sua entrada em uso no país e a área de inspeção e fiscalização responsável pela avaliação das Boas Práticas de Fabricação".
Atualmente, o Brasil utiliza os imunizantes da Pfizer, AstraZeneca/Oxford, Janssen e CoronaVac para vacinar a sua população adulta. Já no caso das crianças e adolescentes, a Anvisa autorizou o uso da dose pediátrica da Pfizer para pessoas de 5 a 11 anos, e CoronaVac, de 6 a 17 anos.
















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.