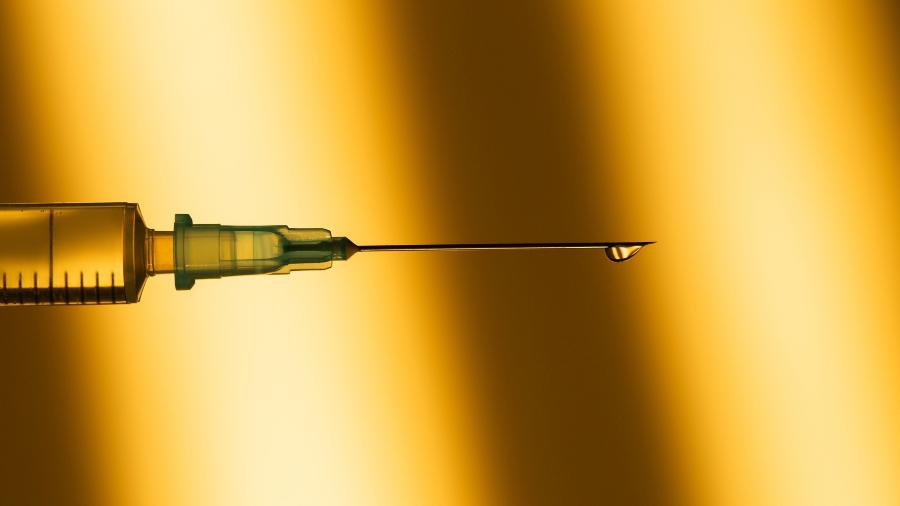
Pfizer pede autorização nos EUA para uso emergencial de vacina contra covid-19

(Reuters) - A Pfizer Inc informou hoje que solicitou aos reguladores de saúde dos Estados Unidos a autorização de uso de emergência de sua vacina contra covid-19, um passo importante para fornecer proteção contra o coronavírus aos norte-americanos já cansados da pandemia.
O pedido feito ao órgão regulador norte-americano, a Food and Drug Administration (FDA, na sigla em inglês), veio poucos dias depois que a Pfizer e a parceira alemã BioNTech relataram os resultados finais do ensaio que mostraram que a vacina foi 95% eficaz na prevenção da covid-19.
As ações da Pfizer subiram 2% e as da BioNTech 5% após a notícia de que a vacina pode estar disponível em breve, o que criou a esperança de um fim da pandemia que já cobrou mais de 250 mil vidas nos EUA e mais de 1,3 milhão em todo o mundo.
As empresas acreditam que a FDA concederá a autorização em meados de dezembro e disseram que começam a enviar as doses quase de imediato. A Pfizer disse crer que terá 50 milhões de doses da vacina prontas neste ano, o suficiente para proteger 25 milhões de pessoas.
Um comitê de aconselhamento da FDA cogita se reunir entre 8 e 10 de dezembro para debater a vacina, disse uma fonte a par da situação à Reuters, mas as datas ainda podem mudar.
Os dados do teste final revelaram que a vacina proporcionou um nível de proteção semelhante em idades e etnicidades diferentes, um sinal promissor, dado que a doença afeta desproporcionalmente idosos e minorias.
(Por Vishwadha Chander em Bengaluru)















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.