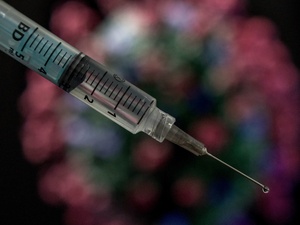
CDC autoriza uso da vacina da Moderna contra a covid-19 nos EUA
Acatando a recomendação de um comitê consultivo, o CDC (Centro de Controle e Prevenção de Doenças, na sigla em inglês) aprovou hoje o uso emergencial da vacina contra a covid-19 desenvolvida pela Moderna nos Estados Unidos. O imunizante é o segundo a receber esse tipo de autorização no país — o primeiro foi o da Pfizer/BioNTech, que já começou a ser distribuído e aplicado.
Agora, o ACIP (Comitê Consultivo em Práticas de Imunização, na sigla em inglês) deve definir quais grupos serão acrescentados às prioridades para vacinação. Com o imunizante da Pfizer, profissionais de saúde e idosos que vivem em casas de repouso foram os primeiros da lista.
Remessas da vacina da Moderna começaram hoje a deixar os locais de armazenamento em direção a mais de 3.700 instalações de saúde em todos os EUA, em um esforço para distribuir a segunda vacina aprovada no país e ampliar a campanha de imunização que começou com a vacina da Pfizer.
O líder do programa de vacina contra o coronavírus dos EUA, Moncef Slaoui, afirmou que o mais provável é que a primeira dose da vacina da Moderna, que foi aprovada pela FDA (Agência de Alimentos e Medicamentos, equivalente à Anvisa) na sexta-feira (18), seja aplicada amanhã de manhã.
"Estamos ansiosos pela vacina. Será um pouco mais fácil distribui-la porque não exige temperaturas tão baixas quanto a da Pfizer [para armazená-la]", comemorou Slaoui à CNN.
Alguns estados estão escolhendo a vacina da Moderna para áreas rurais porque elas podem ser armazenadas por 30 dias em refrigeradores padrões. O imunizante da Pfizer precisa ser transportado e armazenado a -70ºC e dura apenas cinco dias em refrigeradores com temperaturas padrões.
O governo norte-americano planeja entregar 5,9 milhões de doses da Moderna e 2 milhões da Pfizer na próxima semana. Mas o ambicioso objetivo de dar a primeira das duas doses necessárias para 20 milhões de pessoas antes do fim do ano pode se estender à primeira semana de janeiro, disse o general do Exército Gustave Perna, que coordena a operação de distribuição de doses.
O começo da entrega da vacina da Moderna ampliará de maneira significativa a disponibilidade da vacina no momento em que as mortes nos EUA causadas pela covid-19 chegaram a mais de 316 mil nos 11 meses desde o primeiro caso documentado no país.
Vacinas no Brasil
Quatro potenciais vacinas contra a covid-19 estão sendo testadas no Brasil: a vacina da Universidade de Oxford, desenvolvida em parceria com a AstraZeneca; a CoronaVac, do laboratório chinês Sinovac com o Instituto Butantan; a vacina da Pfizer junto à BioNTech; e a vacina do laboratório belga Janssen-Cilag.
Todas se encontram em fase final de testes clínicos, a chamada fase 3, e já submeteram alguns resultados de todo o processo de estudos para a Anvisa (Agência Nacional de Vigilância Sanitária), responsável pela regulação de vacinas e medicamentos no Brasil.
O estudo clínico de uma vacina é dividido em algumas etapas, que vão desde a fase exploratória ou laboratorial, quando ainda são avaliados os componentes para uma melhor formulação da vacina; passam pela fase pré-clínica, quando são feitos testes em animais; chegando por fim à fase clínica. Esta, por sua vez, é subdividida em outras três etapas: as fases 1, 2 e 3.
(Com Reuters)















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.