Senado aprova MP que dá 7 dias à Anvisa para decidir se aprova vacinas
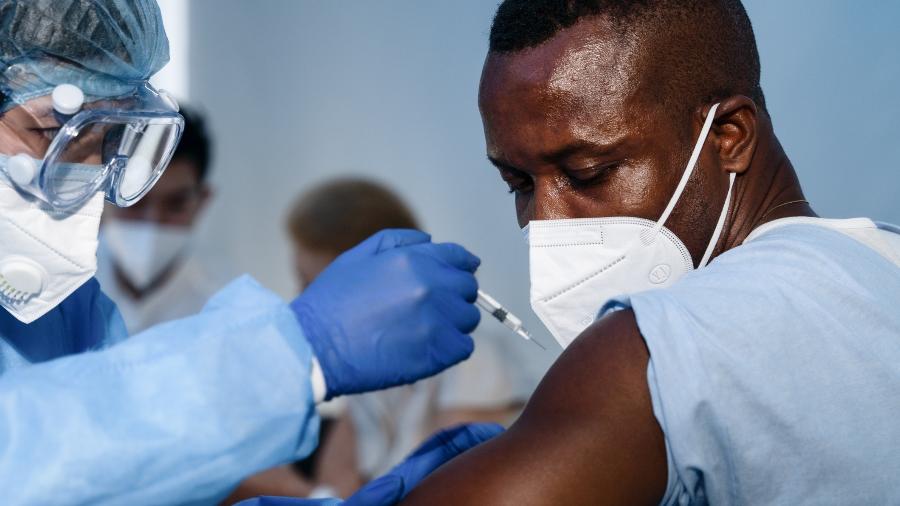
O Senado Federal aprovou hoje o PLV (Projeto de Lei de Conversão) 1/2021, originário da MP (Medida Provisória) 1.026, que facilita a compra e registro de vacinas contra a covid-19, com dispensa de licitação e regras flexíveis para compra de insumos para imunização. O texto também dá sete dias para que a Anvisa (Agência Nacional de Vigilância Sanitária) decida se aprova ou não uma vacina para uso emergencial no Brasil.
A MP foi aprovada por unânimes 73 votos e sem alterações no mérito, após recomendação do relator da proposta, senador Randolfe Rodrigues (Rede-AP). Caso o texto fosse modificado pelos senadores, ele teria que voltar à Câmara dos Deputados para ser apreciado novamente.
A proposta agora vai à sanção do presidente Jair Bolsonaro (sem partido).
O projeto inclui "medidas excepcionais" relativas à compra de vacinas, de bens e serviços de logística, de tecnologia da informação e comunicação, de comunicação social e publicitária e de treinamentos destinados à vacinação contra a covid-19 e sobre o plano nacional de imunização.
A MP determina que a aplicação de vacinas deve seguir o cronograma nacional, elaborado pelo Ministério da Saúde, e autoriza estados e municípios a comprar e aplicar imunizantes caso a União não adquira doses suficientes para os grupos prioritários previstos. Este último ponto acompanha o entendimento do STF (Supremo Tribunal Federal) sobre o tema.
O projeto ainda dá prazo de sete dias para a Anvisa (Agência Nacional de Vigilância Sanitária) decidir sobre a autorização para uso emergencial de vacinas que tenham sido aprovadas em outros países, em uma lista que considera desde os Estados Unidos até a Índia. Até então, esse prazo era de dez dias caso a vacina tivesse passado por estudos de fase 3 no Brasil.
O dispositivo foi desenhado para facilitar a aprovação da Sputnik V, desenvolvida pelo Instituto Gamaleya (Rússia), e da Covaxin, do laboratório Bharat Biotech (Índia). A MP dispensa a necessidade da conclusão da fase 3, mas exige relatório técnico das autoridades internacionais que comprove os padrões de qualidade do produto.
As duas vacinas, porém, ainda não têm autorização da Anvisa para serem utilizadas no Brasil. A União Química e a Precisa Medicamentos, representantes do Gamaleya e do Bharat Biothec no país, ainda devem enviar documentos para que a agência abra seu prazo de análise.
Houve forte lobby para facilitar a entrada desses imunizantes. A União Química tem na linha de frente o dono da empresa, Fernando Marques, candidato derrotado ao Senado nas últimas eleições, o ex-deputado Rogério Rosso e o ex-diretor da Anvisa Fernando Mendes.
Já a Precisa Medicamentos, segundo revelado pelo Estadão/Broadcast, tem como sócia a Global Gestão em Saúde, que deve R$ 20 milhões ao Ministério da Saúde por descumprir contrato feito na gestão de Ricardo Barros (PP-PR), atual líder do governo na Câmara. Foi Barros quem apresentou emenda para a agência da Índia ser considerada na MP 1.026, mas ele nega favorecimento à empresa.
(Com Agência Senado, Estadão Conteúdo e Reuters)

















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.