Secretário da Bahia: Sputnik chegará ao país uma semana após aval da Anvisa

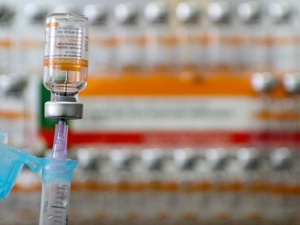
O secretário de Saúde da Bahia, Fábio Vilas-Boas, disse hoje que as primeiras doses da Sputnik V, vacina contra covid-19 do laboratório russo Gamaleya, devem chegar ao Brasil uma semana após a autorização da Anvisa (Agência Nacional de Vigilância Sanitária).
Na última quinta-feira (1), a agência recebeu pedidos de importação do imunizante de nove estados: Bahia, Acre, Rio Grande do Norte, Maranhão, Mato Grosso, Piauí, Ceará, Pernambuco e Sergipe.
Em entrevista à TV Bahia, Vilas-Boas disse que o diretor-presidente da Anvisa, Antonio Barra Torres, pediu uma reunião para amanhã com os governadores para tratar sobre o assunto.
"Os governadores do Nordeste enviaram para a Anvisa uma carta solicitando autorização para importação. Esse documento legal... É preciso ser emitido a autorização pela Anvisa. O diretor-presidente da Anvisa, Almirante Barra Torres, solicitou uma reunião para amanhã com os governadores para alinhar esse processo", disse.
"Vamos ver o que a Anvisa vai dizer, depende dela a partir de agora, a autorização. Saindo a autorização, em uma semana a vacina está aqui no Brasil", acrescentou ele.
O governador da Bahia, Rui Costa (PT), anunciou em março que o contrato para a compra da vacina russa foi assinado e prevê a aquisição de 9,7 milhões de doses. O acordo faz parte de uma negociação do Consórcio Nordeste com o Fundo de Investimentos Diretos da Rússia, que fornecerá 37 milhões de doses ao Brasil.
O pedido de uso emergencial no Brasil da Sputnik V foi recebido pela Anvisa no dia 26 de março. Mas diante da ausência de documentos considerados importantes, a agência suspendeu, no dia seguinte, o prazo de análise do pedido de autorização para uso emergencial.
Na última quarta-feira (31), a agência recebeu uma complementação ao pedido para uso emergencial da vacina, mas ainda faltavam documentos e o prazo de análise segue suspenso.
Segundo a nota da agência reguladora divulgada na ocasião, os documentos recebidos fazem parte de item que trata dos requisitos mínimos para autorização de uso emergencial, que "trata da lista de todos os locais onde a vacina está ou será fabricada, e as documentações relacionadas às Boas Práticas de Fabricação (BPF) dos locais de fabricação".
A Anvisa acrescentou, no entanto, que ainda falta a entrega de documentos relacionados a outros itens que também tratam de Boas Práticas de Fabricação, razão pela qual "o prazo de sete dias úteis permanece suspenso até a apresentação da documentação faltante". De qualquer forma, a agência esclareceu que o material já enviado é avaliado pela equipe.















ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.