EUA: Agências recomendam suspensão em aplicação da vacina Johnson & Johnson
As principais autoridades de saúde dos Estados Unidos recomendaram a suspensão do uso da vacina contra a covid-19 da Johnson & Johnson, feita por sua unidade farmacêutica Janssen, por precaução enquanto investigam se o imunizante produz coágulos de sangue.
A agência regulatória de Alimentos e Medicamentos dos Estados Unidos (FDA) e o Centro de Controle e Prevenção de Doenças (CDC) estão avaliando a "importância potencial" de seis casos reportados de um tipo "raro e grave" de coágulos sanguíneos no país.
Em um comunicado conjunto, os órgãos informaram que os seis casos ocorreram em mulheres com idades entre 18 e 48 anos, e os sintomas ocorreram 6 a 13 dias após a vacinação. Ao todo, mais de 6,8 milhões de doses do imunizante já foram aplicadas nos Estados Unidos.
Nos casos, um tipo de coágulo sanguíneo chamado trombose de seios venosos cerebrais foi detectado em combinação com baixo nível de plaquetas sanguíneas. O CDC e a FDA disseram que os eventos adversos parecem ser extremamente raros.
"O CDC irá convocar uma reunião do Comitê Consultivo em Práticas de Imunização (ACIP) na quarta-feira (14) para revisar esses casos e avaliar sua importância potencial", diz o comunicado.
"O FDA vai revisar essa análise, pois também investiga esses casos. Até que o processo seja concluído, estamos recomendando uma pausa no uso desta vacina por cautela", completa.
A J&J disse estar trabalhando próxima dos reguladores e afirmou que nenhuma relação causal clara foi estabelecida entre os eventos e a vacina. Uma mulher morreu e uma segunda no Estado do Nebraska foi hospitalizada em estado grave, disse o jornal The New York Times citando autoridades.
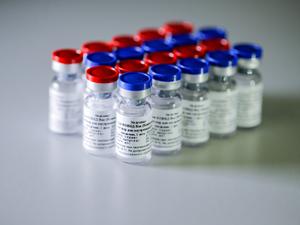
Vacina em dose única
A vacina é produzida pela Janssen, empresa farmacêutica da Johnson & Johnson. Ela é administrada em dose única e foi autorizada para uso emergencial nos Estados Unidos no final de fevereiro, após os imunizantes das farmacêuticas Pfizer/BioNTech e Moderna receberem luz verde.
No Brasil, a vacina teve o uso emergencial aprovado pela Anvisa (Agência Nacional de Vigilância Sanitária) no dia 31 de março, mas ainda não está sendo aplicada.
O governo brasileiro firmou um acordo com a Janssen para entrega de 38 milhões de doses até o último trimestre de 2021.
*Com informações da agência AFP e Reuters














ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.