Instituto Butantan diz que receberá vacinas prontas da China nesta semana
O diretor do Instituto Butantan, Dimas Covas, afirmou hoje que a instituição receberá vacinas prontas da China ainda nesta semana, e a matéria-prima para a produção da CoronaVac, até o final de novembro.
"Já receberemos vacinas nesta semana. Vamos receber já uma primeira partida de vacinas prontas da China. Também receberemos ainda neste mês um quantitativo inicial de 600 litros de matéria-prima para iniciar a produção aqui no Butantan. Tudo caminha para que rapidamente tenhamos um quantitativo de 46 milhões de doses de vacinas prontas para uso já em janeiro", disse.
Dimas Covas participou de comissão da Câmara dos Deputados que acompanha ações relacionadas à pandemia da covid-19. A reunião hoje foi para tratar da CoronaVac, vacina em desenvolvimento pelo laboratório chinês Sinovac em parceria com o Instituto Butantan e alvo de embates.
Em 20 de outubro, o Ministério da Saúde anunciou que compraria 46 milhões de doses da CoronaVac. Um dia depois, o presidente Jair Bolsonaro (sem partido) desautorizou o ministro da Saúde, Eduardo Pazuello, e suspendeu a compra. Desde então, a situação da compra da CoronaVac pelo governo federal está indefinida. Covas ressaltou que, historicamente, o Butantan trabalha em função do SUS (Sistema Único de Saúde).
O diretor do Butantan ressaltou que a vacina precisa ser registrada na Anvisa (Agência Nacional de Vigilância Sanitária) antes de ser distribuída e aplicada à população. O processo está em curso e depende da finalização dos estudos clínicos de fase três, em andamento, com mais de 10 mil voluntários vacinados. É preciso vacinar cerca de mais 2 mil voluntários nessa fase.
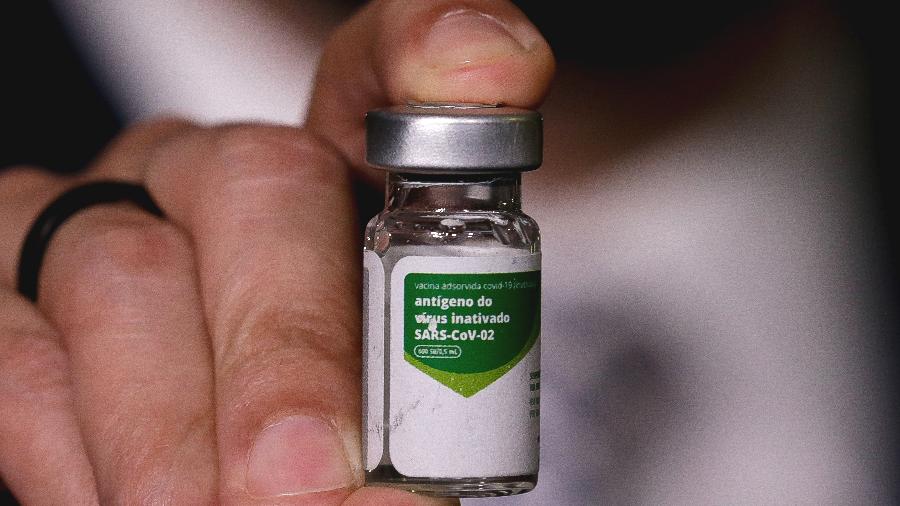
Os resultados serão associados aos dados já existentes de fase um e fase dois realizados na China, além do uso emergencial da vacina autorizado no país asiático, com mais de 60 mil pessoas vacinadas, disse Covas. Ele afirmou que o conjunto de dados aponta para a segurança do produto, baseado no vírus inativado.
Ainda não há previsão concreta para o término dos estudos clínicos e a emissão da autorização pela Anvisa.
Suspensão e retorno dos testes
Após críticas do Instituto Butantan à forma como foi comunicada pela Anvisa a suspensão dos testes da CoronaVac, Dimas Covas disse haver um "entendimento muito bom com a agência do ponto de vista técnico" em relação à vacina.
Ele citou avanços relacionados à inspeção de boas práticas de fabricação a ser realizada na China, por exemplo. Tanto o Butantan como a Anvisa estão com técnicos no país. Os da Anvisa cumprem quarentena para fazer uma inspeção na unidade que produz a matéria-prima que será recebida ainda em novembro.
Hoje, deputados federais cobraram uma maior clareza na comunicação da Anvisa ao suspender testes em decorrência de efeitos adversos graves, como foi feito em relação à CoronaVac. Para os parlamentares presentes à comissão hoje, houve uma falha da agência à época ao avisar o Butantan da atitude por e-mail tarde da noite e, cerca de 40 minutos depois, publicar a decisão em seu portal para torná-la pública.
Os deputados também criticaram a politização ocorrida em seguida. O presidente Jair Bolsonaro (sem partido) usou as redes sociais para atacar o governador de São Paulo, João Doria (PSDB) e dizer que "ganhou mais uma". O Butantan criticou a interrupção determinada pela Anvisa e afirmou que informou que a morte de um dos voluntários da pesquisa não tem ligação direta com a vacina.
Na avaliação de alguns deputados, a politização só ocorreu porque a Anvisa não resolveu esperar o dia seguinte para conversar com o Butantan, em reunião já pré-marcada, e entender melhor o que seria esse efeito adverso grave inesperado. Dois dias depois da suspensão, com reuniões e chegada de mais documentos, a Anvisa liberou a retomada dos testes.
A relatora da comissão, deputada Carmen Zanotto (Cidadania-SC), quer recomendar uma conduta única na comunicação para quando ocorrerem efeitos adversos e disse que, às vezes, um telefonema resolve possíveis conflitos desnecessários.
"A minha recomendação como relatora seria que se evite ao máximo qualquer tipo de informação externa sem que antes se tenha clareza dos fatos e que as partes sejam comunicadas. Quando as partes não são comunicadas, a gente acaba tendo na imprensa o debate desnecessário", disse.
O gerente-geral de Medicamentos e Produtos Biológicos da Anvisa, Gustavo Mendes Lima Santos, afirmou que o foco da Anvisa é a segurança dos participantes e a confiabilidade da vacina. Quando a agência foi comunicada sobre um problema com um dos voluntários, o relato era ainda muito simples, sem informações consideradas importantes, disse. Por exemplo, boletim de ocorrência, posicionamento de comitê independente de segurança e laudos complementares.
Gustavo afirmou que a Anvisa se pautou pela cautela e com o "máximo de zelo" e justificou que, se a Anvisa não tivesse tomado uma decisão no sentido da suspensão e, depois, se revelasse que a morte estava diretamente ligada à CoronaVac, seria cobrada por uma eventual inação. Ele defendeu que, nesses processos, não cabem informalidades e que a formalidade e transparência trazem a segurança necessária, inclusive à população.
O gerente negou que tenha havido interferência política, assim como o presidente-diretor da Anvisa, Antonio Barra Torres, que também participou da reunião.
















Seja o primeiro a comentar
Essa área é exclusiva para você, assinante, ler e comentar.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.