Anvisa libera uso emergencial da Coronavac para crianças de 3 a 5 anos
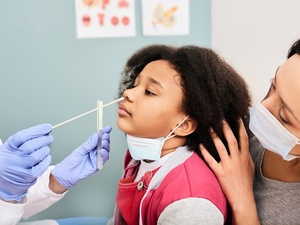
Por maioria, a Anvisa (Agência Nacional de Vigilância Sanitária) liberou hoje o uso emergencial da vacina Coronavac contra a covid-19 para crianças de 3 a 5 anos. Até então, o imunizante era autorizado apenas para crianças a partir de 6 anos.
A recomendação da Área Técnica da Anvisa para a faixa etária é de um esquema vacinal de duas doses, com intervalo de 28 dias, e mesma dose usada para adultos. Crianças imunocomprometidas não devem ser vacinadas por falta de informações sobre a aplicação no grupo.
A votação da diretoria foi aberta pela relatora, a diretora Meiruze Freitas, que se posicionou favorável à ampliação da vacinação. Depois, os diretores Rômison Mota, Antonio Barra Torres e Alex Machado e a diretora Cristiane Rose Jourdan acompanharam o voto.
Meiruze citou os benefícios da imunização para o grupo, e ressaltou a importância para redução de casos graves, complicações e sequelas causadas pela doença, bem como de mortes. A relatora reforçou o pedido para que o Butantan continue enviando dados de estudos e acompanhamento da faixa etária.
"Assim, mesmo considerando as limitações e incertezas relatadas pela área técnica, permitir que os gestores de saúde façam a avaliação do real custo de efetividade de usar a Coronavac, bem como o direito dos pais que desejam vacinar os seus filhos, passa pelo escopo dessa avaliação", disse a diretora.
A Coronavac foi a primeira vacina a ser aplicada no Brasil para iniciar a imunização dos brasileiros contra a doença. O imunizante está em uso emergencial desde 17 de janeiro do ano passado.
O gerente-geral de medicamentos e produtos biológicos da Anvisa, Gustavo Mendes, se mostrou a favor da liberação. O servidor considerou que os dados de efetividade obtidos em pesquisa mostram uma importante efetividade contra a hospitalização das crianças. Ele lembrou que sociedades médicas relacionadas ao tema consideram que os benefícios da vacinação superam os riscos.
Mendes também ressaltou que os dados são indicativos, porque devem ser ampliados. Ele ressaltou a necessidade de seguir com estudos para informações sobre a duração da proteção e potenciais doses de reforço.
Já Helaine Capucho, da GFARM (Gerência de Farmacovigilância), recomendou a criação de um plano de comunicação de riscos. Ela lembrou a importância da notificação de qualquer evento adverso pós-vacina nos canais oficiais da agência.
Durante a reunião, além dos diretores da Anvisa, participaram pesquisadores como Valéria Valim, professora de Medicina da Hucam-UFES/EBSERH e coordenadora dos estudos sobre a efetividade da Coronavac. Rafaella Fortini, da Fiocruz em Minas Gerais, também coordenou estudos e falou sobre a efetividade para crianças de 3 a 5 anos.
Manoel Barra, da Fiocruz da Bahia, falou sobre os dados de efetividade e apresentou informações sobre adolescentes e crianças. Já Marco Aurélio Sáfadi, da Santa Casa de SP, falou sobre a importância da ampliação da vacinação e dos estudos continuados sobre a aplicação.
A agência recebeu no início de junho os dados adicionais referentes à solicitação para aplicação nessa faixa etária. A primeira reunião sobre a ampliação do uso entre a Anvisa e o Butantan foi em março, e um mês depois foram pedidas informações adicionais, alegando que os estudos enviados eram insuficientes.
Na última sexta-feira (8), a agência recebeu um pedido do Instituto Butantan para registro definitivo do imunizante. O prazo para a análise do pedido é de 60 dias.
Coronavac teve produção suspensa
No fim de junho, o Butantan informou que a Coronavac teve sua produção suspensa. Isso aconteceu, segundo o instituto, por falta de novos pedidos de lotes do imunizante. No total, o Butantan disse ter entregue mais de 110 milhões de doses ao Ministério da Saúde. O último envio ocorreu em fevereiro deste ano. Desde então, não houve procura para novos contratos.
Hoje, após a aprovação da Anvisa para a faixa etária de 3 a 5 anos, o Butantan afirmou que espera agora que o imunizante seja incorporado ao Programa Nacional de Imunizações (PNI) do Ministério da Saúde, de acordo com a demanda necessária e mediante contratação. Ainda de acordo com o instituto, além do Chile, outros países como China, Colômbia, Tailândia, Camboja, Equador e o território autônomo de Hong Kong já administram a CoronaVac em crianças de três anos ou mais.














ID: {{comments.info.id}}
URL: {{comments.info.url}}
Ocorreu um erro ao carregar os comentários.
Por favor, tente novamente mais tarde.
{{comments.total}} Comentário
{{comments.total}} Comentários
Seja o primeiro a comentar
Essa discussão está encerrada
Não é possivel enviar novos comentários.
Essa área é exclusiva para você, assinante, ler e comentar.
Só assinantes do UOL podem comentar
Ainda não é assinante? Assine já.
Se você já é assinante do UOL, faça seu login.
O autor da mensagem, e não o UOL, é o responsável pelo comentário. Reserve um tempo para ler as Regras de Uso para comentários.